��Ŀ����
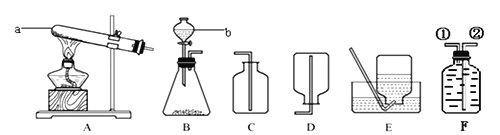
����Ŀ��ij��ȤС��ͬѧΪ��Ū�弴��ά��������������ijɷ֣�����ˮ���ռ�һƿ������Ʒ����������ͼʵ�����̽����й�̽�����

(1)��������a��Ϊʯ��ˮ����ǣ���˵�������к���_____����(�ѧʽ)��
(2)����ڵ�Ŀ����________��д����Ӧ�еĻ�ѧ����ʽΪ______��
(3)��������b��Ϊ������ˮ�����֣�����֤��������Ʒ��һ��������Ԫ�أ�������______��Ҫ�ų����ָ��ſɲ�ȡ�Ĵ�ʩ��______��
(4)��ȡ(3)�е��ų����Ŵ�ʩ���ٽ��м���̽������������a��c����Ϊʯ��ˮ����ǣ�������b��Ϊ������ˮ������֤��������������ijɷ���һ������____��____����д����صĻ�ѧ����ʽ____
���𰸡�CO2 Ϊ�˳�ȥ������Ʒ�еĶ�����̼ CO2+2NaOH�TNa2CO3+H2O �����ռ���������Ʒ�б�������ˮ���������ռ����岻һ��������Ԫ�� �ڵ�ȼ�ļ����ǰ��װһ������װ��(������м�ʯ�һ�Ũ����) ������̼ ���� CH4��2O2![]() CO2��2H2O ��CO2 ��Ca(OH)2��CaCO3����H2O
CO2��2H2O ��CO2 ��Ca(OH)2��CaCO3����H2O
��������
��1��������̼��ʹ����ʯ��ˮ����ǣ���������a��Ϊʯ��ˮ����ǣ���˵�������к���CO2���塣
��2������������Һ������Ϊ�����ն�����̼���壬�Է��������飻���������������̼��Ӧ����̼���ƺ�ˮ��д����Ӧ�еĻ�ѧ����ʽΪCO2+2NaOH�TNa2CO3+H2O��
��3����������b��Ϊ������ˮ�����֣�����֤��������Ʒ��һ��������Ԫ�أ������������ռ���������Ʒ�б�������ˮ��������������Ʒ�в�һ��������Ԫ�أ�Ҫ�ų����ָ��ſɲ�ȡ�Ĵ�ʩ���ڵ�ȼ�ļ����ǰ��װһ������װ��(������м�ʯ�һ�Ũ����)
��4����ȡ��3���е��ų����Ŵ�ʩ���ٽ��м���̽������������a��c����Ϊʯ��ˮ����ǣ�������b��Ϊ������ˮ������֤��������������ijɷ���һ�����ж�����̼�ͼ��顣����ȼ�����ɶ�����̼��ˮ����Ӧ����ʽΪ��CH4��2O2![]() CO2��2H2O��������̼��ʹ����ʯ��ˮ����ǣ���Ӧ����ʽΪ��CO2 ��Ca(OH)2��CaCO3����H2O��
CO2��2H2O��������̼��ʹ����ʯ��ˮ����ǣ���Ӧ����ʽΪ��CO2 ��Ca(OH)2��CaCO3����H2O��

 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�����Ŀ���ҹ�������ѧ�Һ�°����������ˡ������Ƽ������ԭ������Ҫ��һ������ʳ��ˮ���Ⱥ�ͨ������NH3��CO2�Ʊ�NaHCO3����ѧ����ʽ��NaCl+ NH3+CO2+H2O= NaHCO3��+NH4Cl
ij��ȤС����ʵ����ģ��ù��̣����Ͼ���IJ���ش��������⣺
I�������Ʊ�
��1��������̼�����Ʊ�
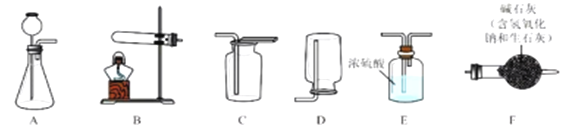
ʵ���ҳ�����ʯ��ʯ��ϡ���ᷴӦ�Ʊ�CO2���仯ѧ����ʽΪ_____________��Ӧѡ��������ռ�װ��Ϊ______(ѡ��װ�ö�Ӧ����ĸ)��
��2�������Ʊ�
ʵ���ҳ����������հ�������ֹ��Ⱦ������ʵ�����Ʊ�NH3�ķ�Ӧԭ��Ϊ��Ca(OH)2(��)+2NH4Cl(��) ![]() CaCl2+2H2O+2NH3������Ҫ�Ʊ�������NH3����ѡװ�õ���ȷ����˳��Ϊ_____��______(ѡ��װ�ö�Ӧ����ĸ)��ʵ�����Ʊ�O2Ҳ���������Ʊ�NH3�ķ���װ�ã�д���ø÷���װ���Ʊ�O2�Ļ�ѧ����ʽ__________��
CaCl2+2H2O+2NH3������Ҫ�Ʊ�������NH3����ѡװ�õ���ȷ����˳��Ϊ_____��______(ѡ��װ�ö�Ӧ����ĸ)��ʵ�����Ʊ�O2Ҳ���������Ʊ�NH3�ķ���װ�ã�д���ø÷���װ���Ʊ�O2�Ļ�ѧ����ʽ__________��
II��NaHCO3�Ʊ�
���� | NaHCO3 | NH4Cl |
�ܽ��/g(20��) | 9.6 | 37.2 |
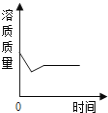
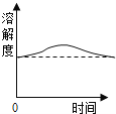
��3�����ݱ����е��ܽ�����ݣ�����20��������NaHCO3�ܹ��ȴ���Һ�нᾧ������ԭ��________��
��4���ù�������һ����NH4Cl��ũҵ�����г�������______________��