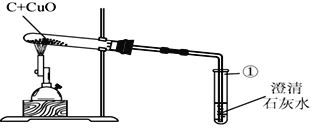
��Ŀ����
����Ŀ����п��Һ����п������п��������Ҫ����;��
I���Ժ�п��Һ����Ҫ�ɷ�Ϊ ![]() ������Ϊ
������Ϊ ![]() ��
�� ![]() ��Ϊԭ���Ʊ���ˮ����п��
��Ϊԭ���Ʊ���ˮ����п�� ![]() �����������¡�
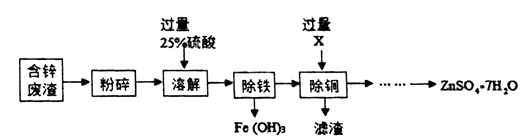
�����������¡�
��1�������Ŀ������
��2������X��һ�ֽ������ʣ���X�����ѧʽ������ͭʱ�����ķ�Ӧ������Ӧ���������Ӧ���ͣ���
��3����ˮ����п���ܽ����������������ơ������л����ˮ����пǰʡ�ԵIJ����Ǽ���Ũ���������ˡ�ϴ�Ӻ͵��º�ɡ�
II����ij��п�� ![]() ����Ϊ62.5%��Ϊԭ���Ʊ�п��һ�ַ����ǣ���־�����뷴Ӧ�����Ƚ���̿����п����
����Ϊ62.5%��Ϊԭ���Ʊ�п��һ�ַ����ǣ���־�����뷴Ӧ�����Ƚ���̿����п���� ![]() ʱ���գ�Ȼ���������õ�п����100����������п�����������Ƶ�п�֡�����ʾ��
ʱ���գ�Ȼ���������õ�п����100����������п�����������Ƶ�п�֡�����ʾ�� ![]()
![]() ZnO + CO2����
ZnO + CO2����
���𰸡�
��1������Ӧ��ĽӴ������ʹ��Ӧ����ȫ
��2��Zn���û�
��3�����½ᾧ��32.5
�������������1������ı����Խ��ѧ��Ӧ����Խ�졣��п���������Ŀ��������Ӵ�������ӿ췴Ӧ���ʣ���ַ�Ӧ��
��2�����������X��Ŀ���dz�ȥͭ����С��ʵ�������ʵij��ӣ���Ҫ��ȥ������Ҫ���������µ����ʣ����ǵ��������˳��X������п����������п���û���ͭ�������Ӧ�������û���Ӧ��
��3����������Թ����Һ��ķ������Ƚ��ȵı�����Һ��ȴ������ͻ������������о��������ı�����Һ�����ˣ���������ˮϴ�ӣ��ٵ��º�ɡ����Բ����IJ����ǣ�����Ũ������ȴ�ᾧ�����ˣ�ϴ�Ӻ͵��º�ɡ� II.��ĿҪ���������������Ƶ�п���ٶ֣���������������Ƶ�п������ΪX��
���������֪ZnCO3��������=100t��62.5%=62.5t![]()
![]() ZnO + CO2��
ZnO + CO2�� ![]()
![]() ZnO + CO2������������ʽ��֪��
ZnO + CO2������������ʽ��֪��
ZnCO3~ | Zn |
125 | 65 |
62.5t | x |
![]()
x=32.5t.
�ʴ�Ϊ����1������Ӧ��ĽӴ������ʹ��Ӧ����ȫ����2��Zn���û�����3�����½ᾧ��32.5.
��1����Ӧ��Ӵ�Խ��֣���Ӧ����Խ�죻
��2�����ݷ�Ӧ������������������жϷ�Ӧ���ͣ�
��3��������Һͨ����ȴ���Դﵽ���壻�ҳ�̼��п��п�Ĺ�ϵʽ������̼��п�������������п������.

 ����ѵ��ϵ�д�
����ѵ��ϵ�д� ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�����Ŀ���������С������ء�֮�ƣ�������ƫ���ԡ��������ﲻ���˽�����ֲ����
���� | ���� | �̽� | ���� | �ʲ� |
��������ֲ������pH��Χ | 5.0-5.5 | 5.0-5.7 | 6.0- 7.0 | 7.2- 8.5 |
A.����
B.�̽�
C.����
D.�ʲ�