题目内容
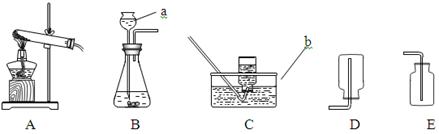
根据下图所示装置回答问题:
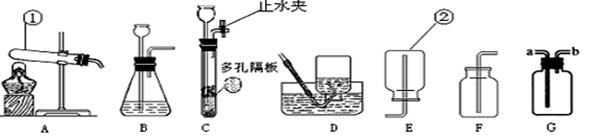
(1)用A装置制取氧气,反应的化学方程式为 。
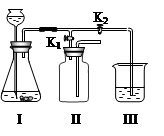
(2)实验室若用B装置来制取二氧化碳时,往长颈漏斗中应加入 。若用G来收集二氧化碳,二氧化碳应从 进(选“a”或“b”)。
(3)制取二氧化碳最好选择的发生装置是 (选择“B”或“C”),与另一个装置相比,其优点是: 。
(4)硫化氢是一种无色且有臭鸡蛋气味的气体,能溶于水,实验室用硫化亚铁跟稀硫酸反应制取硫化氢气体。实验室制取H2S气体时,发生装置应选用 ,收集装置应选用__________ (填仪器编号)。
(5)红旗水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)
有关实验数据如下表:
求该石灰石中碳酸钙的质量分数。

(1)用A装置制取氧气,反应的化学方程式为 。
(2)实验室若用B装置来制取二氧化碳时,往长颈漏斗中应加入 。若用G来收集二氧化碳,二氧化碳应从 进(选“a”或“b”)。
(3)制取二氧化碳最好选择的发生装置是 (选择“B”或“C”),与另一个装置相比,其优点是: 。
(4)硫化氢是一种无色且有臭鸡蛋气味的气体,能溶于水,实验室用硫化亚铁跟稀硫酸反应制取硫化氢气体。实验室制取H2S气体时,发生装置应选用 ,收集装置应选用__________ (填仪器编号)。
(5)红旗水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)
有关实验数据如下表:
| | 反应前 | 反应后 | |
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 160 g | 12 g | 167.6 g | |
求该石灰石中碳酸钙的质量分数。
(1)2KMnO4 △ K2MnO4 + MnO2 + O2↑ 或 2KClO3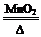 2KCl + 3O2 ↑
2KCl + 3O2 ↑
(2)稀盐酸、a (3)C、可随时控制反应的发生与停止 (4)B或C、F (5)83.3%
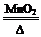 2KCl + 3O2 ↑
2KCl + 3O2 ↑(2)稀盐酸、a (3)C、可随时控制反应的发生与停止 (4)B或C、F (5)83.3%
试题分析:(1)用A装置制取氧气,是加热高锰酸钾或者氯酸钾制取氧气,反应的化学方程式为2KMnO4 △ K2MnO4 + MnO2 + O2↑或 2KClO3
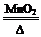 2KCl + 3O2 ↑。
2KCl + 3O2 ↑。(2)实验室若用B装置来制取二氧化碳时,往长颈漏斗中应加入稀盐酸。若用G来收集二氧化碳,二氧化碳应从a进入,因为二氧化碳密度大于空气。
(3)制取二氧化碳最好选择的发生装置是C,与另一个装置相比,其优点是:可随时控制反应的发生与停止。
(4)硫化氢是一种无色且有臭鸡蛋气味的气体,能溶于水,实验室用硫化亚铁跟稀硫酸反应制取硫化氢气体。实验室制取H2S气体时,发生装置应选用B或C,收集装置应选用F。
(5)由题中数据可知,反应前后,各物质的质量总和的差值就是反应产生的二氧化碳的质量,即二氧化碳的质量为160g+12g-167.6g=4.4g。
解:设该石灰石中碳酸钙的质量为X。
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
100 44
X 4.4g
100:44=X:4.4g
X=10g
该石灰石中碳酸钙的质量分数为
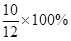 =83.3%。
=83.3%。答:该石灰石中碳酸钙的质量分数为83.3%。
点评:选择制取气体的装置,要根据反应物的状态和反应条件,以及气体的性质来选择合适的实验装置。
根据化学方程式计算,要注意解题的步骤,设、写、找、列、解、答。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目