题目内容
在实验室里,通常用铁与盐酸(HCl)反应制取氢气,同时还有氯化亚铁生成.
(1)写出该反应的化学方程式 .
(2)实验室里用5.6g铁与足量盐酸反应,可制得氢气和氯化亚铁的质量各是多少?
(1)写出该反应的化学方程式
(2)实验室里用5.6g铁与足量盐酸反应,可制得氢气和氯化亚铁的质量各是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:铁和稀盐酸反应生成氯化亚铁和氢气;
根据铁的质量可以计算反应生成氢气和氯化亚铁的质量.
根据铁的质量可以计算反应生成氢气和氯化亚铁的质量.
解答:解:(1)铁和稀盐酸反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故填:Fe+2HCl═FeCl2+H2↑.
(2)设生成氯化亚铁、氢气的质量分别是x、y,
Fe+2HCl═FeCl2+H2↑,
56 127 2
5.6g x y
=
=
,
x=12.7g,y=0.2g,
答:生成氯化亚铁、氢气的质量分别是12.7g、0.2g.
故填:Fe+2HCl═FeCl2+H2↑.
(2)设生成氯化亚铁、氢气的质量分别是x、y,
Fe+2HCl═FeCl2+H2↑,
56 127 2
5.6g x y
| 56 |
| 5.6g |
| 127 |
| x |
| 2 |
| y |
x=12.7g,y=0.2g,
答:生成氯化亚铁、氢气的质量分别是12.7g、0.2g.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
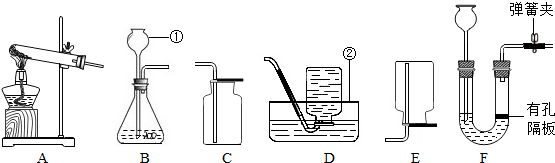
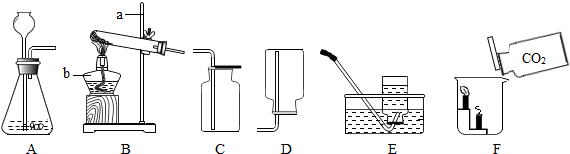

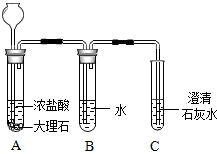 已知同等条件下HCl气体的溶解度大于CO2的溶解度.在实验室制取二氧化碳并检验其性质的实验中,如果用浓盐酸代替稀盐酸,并将产生的气体通入澄清的石灰水,往往看不到溶液变浑浊的现象.现有一同学用如图装置进行实验,却看到了澄清石灰水变浑浊的现象
已知同等条件下HCl气体的溶解度大于CO2的溶解度.在实验室制取二氧化碳并检验其性质的实验中,如果用浓盐酸代替稀盐酸,并将产生的气体通入澄清的石灰水,往往看不到溶液变浑浊的现象.现有一同学用如图装置进行实验,却看到了澄清石灰水变浑浊的现象