题目内容
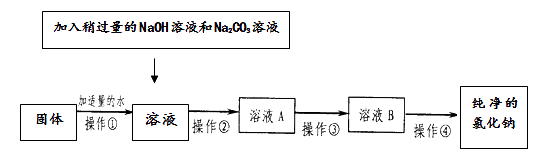
【题目】某化工厂排放的废液中含有大量的硫酸锌和硫酸铜,化学兴趣小组的同学根据所学知识设计了一个方案,用来回收金属铜并得到硫酸锌晶体,主要过程如下图所示:
请回答下列问题:
(1)步骤②中分离物质的方法是。
(2)固体A的成分是。
(3)步骤②中发生反应的化学方程式为 ,
(4)步骤③中加入的B物质是。
【答案】
(1)过滤
(2)锌和铜
(3)Zn+CuSO4=Cu+ZnSO4
(4)稀硫酸
【解析】化工厂排放的废液中含有大量的硫酸锌和硫酸铜,回收金属铜并得到硫酸锌晶体,②③操作后的溶液中溶质都是硫酸锌,向混合液中加入过量锌后,锌与硫酸铜反应生成铜和硫酸锌,是由一中单质和一种化合物生成另一种和另一种化合物的置换反应;所得固体是生成铜和剩余锌的混合物,所根据加B后所得是铜和硫酸锌可知B为硫酸;过滤能将固体和液体分离,所以步骤②中分离物质的方法是过滤。
根据过滤原理分析,过滤能除去液体中不溶的固体;根据金属活动性顺序中,排在前面的金属能与排在后面的金属的盐溶液反应分析。

 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案【题目】现有A、B两种银白色的金属,某同学想要探究这两种金属的活动性。
【设计实验】
取大小相同的两块金属,用砂纸打磨光亮,分别放入两支试管中再加入等量的同种稀盐酸,操作与现象如表:
实验 | 试管1 | 试管2 |
操作 |
|
|
现象 | 金属表面产生气泡较慢 | 金属表面产生气泡较快 |
【思考结论】
(1)通过上述实验,判断出两种金属的活动性顺序是A________B(填“>”或“<”)。
(2)假设其中的一种金属是铁,除观察到铁的表面有气泡产生外,还能观察到反应后的溶液 呈_________(填“浅绿色”或“黄色”)。
(3)实验前用砂纸打磨金属片的目的是___________________________________________。
(4)如果两种金属是镁和铁,还可以用镁和一种化合物的溶液来证明两者的金属活动性强弱,你认为该化合物可以是__________________填化学式)。