题目内容
某市热电厂使用的燃料是含硫较多的煤.该厂附近一所中学的同学经常闻到空气有异味,且空气能见度差.学校研究性学习小组意识到这有可能是该厂排出的废气超标造成的,于是在老师的指导下做了探究实验,请你填写下列空白.
【提出问题】空气里SO2是否超标呢?
【查阅资料】Ⅰ.我国关于SO2在风景区、居民区、工厂区的空气质量标准分别见下表:
| 地 区 | 风景区 | 居民区 | 工厂区 |
| SO2浓度限值(mg/m3) | 0.15 | 0.50 | 0.70 |
【设计实验】同学设计以下步骤来测定空气中SO2的含量.
(1)采集工厂附近的空气样品250L.
(2)将空气样品通过NaOH溶液,加入一定量氧化剂H2O2,使其中Na2SO3完全转化为Na2SO4,反应的化学方程式:________.
(3)再加入过量的BaCl2溶液,经过过滤、洗涤、烘干,称量固体质量为1.2mg.
计算:250L空气样品中SO2的质量为________mg.由空气质量标准可得出结论:该厂排放的SO2________.
(4)简述采集空气样品的方法________.
【发现新问题】考虑到空气中的各种气体成分,有同学认为该实验测得的SO2的含量偏大,其依据及你提出的实验改进方案是________.
【反思与应用】为尽快改善该地区的空气质量,请你提出一条合理化建议:________.
解:【设计实验】(2)反应中氧化剂是双氧水,还原剂是亚硫酸钠,故方程式为:Na2SO3+H2O2=H2O+Na2SO4;
(3)根据反应过程中硫原子守恒思想:SO2→Na2SO3→Na2SO4→BaSO4,故可以根据硫酸钡沉淀的质量确定二氧化硫的质量,设二氧化硫的质量为m,
SO2----BaSO4
64 233
m 1.2mg
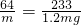 m=0.33mg
m=0.33mg
答:250L空气样品中SO2的质量为0.33mg,0.33mg>0.15mg,超标.
(4)收集气体的方法为:可乐瓶装满水盖上瓶盖拿到工厂附近,然后倒掉水,再盖上瓶盖.
【发现新问题】空气中的二氧化碳也会和二氧化硫一样,经过相应的反应,最终也会转化成碳酸钡沉淀,增加硫酸钡的质量,对实验结果产生影响,根据硫酸钡不溶于酸,二碳酸钡溶于酸的事实,可以向难溶物中加入酸排除二氧化碳的干扰;
【反思与应用】为改善该地区的空气质量,可以将工厂废气进行治理,达标后再排放.
故答案为:
【设计实验】((2)Na2SO3+H2O2═Na2SO4+H2O;(3)0.33、超标;
(4)用可乐瓶装满水盖上瓶盖拿到工厂附近,然后倒掉水,再盖上瓶盖(或用打气管注入;瘪的塑料袋撑起等,其他合理答案也可,但遇水不给分);
【发现新问题】空气中的二氧化碳也要和氢氧化钠溶液反应,并继续与BaCl2溶液反应,生成碳酸钡沉淀.向沉淀中加入过量的稀硝酸后,再进行其余操作;
【反思与应用】工厂废气进行治理,达标后再排放.
分析:【设计实验】(2)根据氧化剂和还原剂之间发生的反应进行书写;
(3)根据反应过程中的原子守恒思想,二氧化硫最后硫元素全部进入硫酸钡中来计算,并进行比较;
(4)根据气体的性质确定气体的收集方法,
【发现新问题】根据空气中的二氧化碳与二氧化硫的性质相似进行分析,可以对二氧化碳的干扰进行屏蔽;
【反思与应用】根据二氧化碳的危害进行解答.
点评:本题综合考查了酸雨的形成、危害,以及二氧化硫及亚硫酸钠的化学性质,并考查了原子守恒思想在解题中的应用,是一道难度较大的综合题目.
(3)根据反应过程中硫原子守恒思想:SO2→Na2SO3→Na2SO4→BaSO4,故可以根据硫酸钡沉淀的质量确定二氧化硫的质量,设二氧化硫的质量为m,
SO2----BaSO4
64 233
m 1.2mg
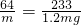 m=0.33mg
m=0.33mg答:250L空气样品中SO2的质量为0.33mg,0.33mg>0.15mg,超标.
(4)收集气体的方法为:可乐瓶装满水盖上瓶盖拿到工厂附近,然后倒掉水,再盖上瓶盖.
【发现新问题】空气中的二氧化碳也会和二氧化硫一样,经过相应的反应,最终也会转化成碳酸钡沉淀,增加硫酸钡的质量,对实验结果产生影响,根据硫酸钡不溶于酸,二碳酸钡溶于酸的事实,可以向难溶物中加入酸排除二氧化碳的干扰;
【反思与应用】为改善该地区的空气质量,可以将工厂废气进行治理,达标后再排放.
故答案为:
【设计实验】((2)Na2SO3+H2O2═Na2SO4+H2O;(3)0.33、超标;
(4)用可乐瓶装满水盖上瓶盖拿到工厂附近,然后倒掉水,再盖上瓶盖(或用打气管注入;瘪的塑料袋撑起等,其他合理答案也可,但遇水不给分);
【发现新问题】空气中的二氧化碳也要和氢氧化钠溶液反应,并继续与BaCl2溶液反应,生成碳酸钡沉淀.向沉淀中加入过量的稀硝酸后,再进行其余操作;
【反思与应用】工厂废气进行治理,达标后再排放.
分析:【设计实验】(2)根据氧化剂和还原剂之间发生的反应进行书写;
(3)根据反应过程中的原子守恒思想,二氧化硫最后硫元素全部进入硫酸钡中来计算,并进行比较;
(4)根据气体的性质确定气体的收集方法,
【发现新问题】根据空气中的二氧化碳与二氧化硫的性质相似进行分析,可以对二氧化碳的干扰进行屏蔽;
【反思与应用】根据二氧化碳的危害进行解答.
点评:本题综合考查了酸雨的形成、危害,以及二氧化硫及亚硫酸钠的化学性质,并考查了原子守恒思想在解题中的应用,是一道难度较大的综合题目.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
某市热电厂使用的燃料是含硫较多的煤.该厂附近一所中学的同学经常闻到空气有异味,且空气能见度差.学校研究性学习小组意识到这有可能是该厂排出的废气超标造成的,于是在老师的指导下做了探究实验,请你填写下列空白.
【提出问题】空气里SO2是否超标呢?
【查阅资料】Ⅰ.我国关于SO2在风景区、居民区、工厂区的空气质量标准分别见下表:
Ⅱ.硫酸钡既不溶于水,也不溶于酸(如不与稀盐酸、稀硝酸等反应).
【设计实验】同学设计以下步骤来测定空气中SO2的含量.
(1)采集工厂附近的空气样品250L.
(2)将空气样品通过NaOH溶液,加入一定量氧化剂H2O2,使其中Na2SO3完全转化为Na2SO4,反应的化学方程式: .
(3)再加入过量的BaCl2溶液,经过过滤、洗涤、烘干,称量固体质量为1.2mg.
计算:250L空气样品中SO2的质量为 mg.由空气质量标准可得出结论:该厂排放的SO2 .
(4)简述采集空气样品的方法 .
【发现新问题】考虑到空气中的各种气体成分,有同学认为该实验测得的SO2的含量偏大,其依据及你提出的实验改进方案是 .
【反思与应用】为尽快改善该地区的空气质量,请你提出一条合理化建议: .
【提出问题】空气里SO2是否超标呢?
【查阅资料】Ⅰ.我国关于SO2在风景区、居民区、工厂区的空气质量标准分别见下表:
| 地 区 | 风景区 | 居民区 | 工厂区 |
| SO2浓度限值(mg/m3) | 0.15 | 0.50 | 0.70 |
【设计实验】同学设计以下步骤来测定空气中SO2的含量.
(1)采集工厂附近的空气样品250L.
(2)将空气样品通过NaOH溶液,加入一定量氧化剂H2O2,使其中Na2SO3完全转化为Na2SO4,反应的化学方程式:
(3)再加入过量的BaCl2溶液,经过过滤、洗涤、烘干,称量固体质量为1.2mg.
计算:250L空气样品中SO2的质量为
(4)简述采集空气样品的方法
【发现新问题】考虑到空气中的各种气体成分,有同学认为该实验测得的SO2的含量偏大,其依据及你提出的实验改进方案是
【反思与应用】为尽快改善该地区的空气质量,请你提出一条合理化建议: