题目内容
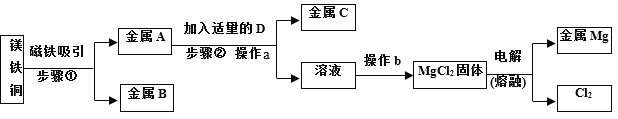
【题目】某金属冶炼厂从含有金属镁、铁、铜的废弃粉末中,分离和回收金属,设计了如下实验方案:
请回答:
(1)步骤①中分离得到的金属B是_____(填化学式);步骤②中加入适量的D是_____(填名称)。
(2)步骤②中操作a的名称是_____;在此过程中需要使用玻璃棒,其作用是_____。
(3)写出步骤②所涉及的化学反应方程式_____。
【答案】Fe 稀盐酸 过滤 引流 Mg+2HCl=MgCl2+H2↑
【解析】
(1)利用磁铁吸引,可以将铁从三种金属粉末中分离出来,所以金属B是铁,其化学式为Fe,故填Fe;
由图可知,金属A中的金属镁与D反应得到氯化镁溶液,则D为稀盐酸,故填稀盐酸。
(2)操作a将金属粉末C于溶液进行了分离,而分离不溶性固体于液体的方法是过滤,固体过滤;
过滤时玻璃棒的作用是引流,故填引流。
(3)由流程图可知,步骤②是镁与稀盐酸反应生成氯化镁和氢气,故反应的化学方程式写为:Mg+2HCl=MgCl2+H2↑。

【题目】现有一包黑色固体粉末,可能含有炭粉、CuO、Fe3O4中的两种或者三种,某化学兴趣小组通过实验探究其成分。
(1)提出问题:该黑色固体粉末成分是什么?
(2)作出猜想:
猜想一:混合固体是炭粉、CuO
猜想二:混合固体是炭粉、Fe3O4
猜想三:混合固体是_____(物质写不去不给分)
猜想四:混合固体是炭粉、CuO、Fe3O4
(3)查阅资料:Fe3O4为黑色粉末,能与盐酸反应,含有Fe3+的盐溶液遇到KSCN(硫氰化钾)溶液时变成红色,Fe(OH)2是一种白色沉淀。
(4)实验探究:取一定量的固体于试管中,加足量的盐酸,充分反应后有部分固体溶解,过滤,得到滤液A,并对滤液A的成分进行如下探究:
实验操作 | 实验现象 | 实验结论 |
步骤一:取一定量滤液A于试管中,加入足量的铁粉 | 无红色固体析出 | 该固体物质一定没有_____ |
步骤二:又取一定量的滤液A于试管中,加入少量的KSCN(硫氰化钾)溶液 | 溶液变成红色 | 滤液A中一定含有的物质是_____ |
步骤三:再取一定量的滤液A于试管中,加入足量的NaOH溶液 | 有红褐色沉淀生成,同时还有少量的白色沉淀生成,白色沉淀迅速变成灰绿色,最后变成红褐色 | 滤液A中还一定含有的物质是_____ |
(5)讨论交流:
①通过以上实验,猜想_____成立。
②写出Fe3O4与盐酸反应的化学方程式:_____。
③四氧化三铁作为铁的一种氧化物,在高温下还能被单质铝还原,同时生成一种稳定的氧化物,请你写出该反应的化学方程式:_____。