题目内容
【题目】“绿水青山就是金山银山”。某工厂产生的废水中含有硫酸锌和少量的硫酸铜以及污泥,为了变废为宝,可利用废水制取七水硫酸锌(ZnSO47H2O),其工艺流程图如图:
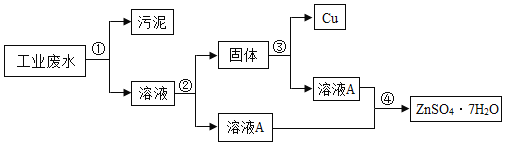
回答下列问题:
(1)步骤①的操作名称是______。
(2)步骤②需加入过量的物质是______(填化学式),其目的是______,反应的化学方程式为______。
(3)步骤③发生反应的基本反应类型为______。
【答案】过滤 Zn 除去硫酸铜 Zn+CuSO4=ZnSO4+Cu 置换反应
【解析】
锌和硫酸铜反应生成硫酸锌和铜,稀硫酸不能和铜反应,能和锌反应生成硫酸锌和氢气。
(1)步骤①是把不溶于水的污泥和液体分离开来,故操作名称是过滤。
(2)锌和硫酸铜反应生成硫酸锌和铜,故步骤②需加入过量的物质是Zn,其目的是除去硫酸铜,反应的化学方程式为Zn+CuSO4=ZnSO4+Cu。
(3)步骤③用稀硫酸除去过量的锌,稀硫酸不能和铜反应,能和锌反应生成硫酸锌和氢气,反应符合一种单质和一种化合物生成另一种单质和另一种化合物,故步骤③发生反应的基本反应类型为置换反应。

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目