题目内容
【题目】近几年我国某些城市酸雨污染较为严重,主要原因是燃烧含硫量高的煤及机动车排放的尾气。
【实验目的】验证煤中含有碳元素,检验是否含有硫元素
【查阅资料】
①已知煤完全燃烧后,其中的碳和硫元素基本都转化成二氧化碳和二氧化硫。
②二氧化碳与高锰酸钾不反应。
③二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),该反应的化学方程式为:
5SO2 + 2KMnO4 + 2H2O = K2SO4 + 2MnSO4 + 2 X ,其中X的化学式是: 。
④二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊,反应的化学方程式为:SO2+Ca(OH)2=CaSO3↓+H2O。
根据上述资料,甲、乙同学进行了如下实验探究。
【实验探究】
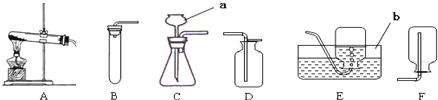
甲同学进行了如下图所示A、B两个实验:


实验现象为 A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
由此甲同学认为:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
乙同学认为甲同学的方案不合理,于是进行了如下图所示实验(夹持装置略去):

【结论与反思】
(1)乙同学认为甲同学的实验方案不合理,其理由是: 。
(2)上图C装置的作用是 。
(3)要证明煤中含有碳元素和硫元素的现象是: 。
【答案】③H2SO4 【结论与反思】(1)二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素
(2)二氧化硫是否除干净(3)B中的溶液褪色,C中的溶液不褪色,D中澄清的石灰水变浑浊
【解析】
试题分析:③根据质量守恒定律的微观解释:在化学反应前后,原子的种类、数目都不变,结合化学反应:5SO2 + 2KMnO4 + 2H2O = K2SO4 + 2MnSO4 + 2 X ,可以推出X化学式为H2SO4
(1)乙同学认为甲同学的实验方案不合理,其理由是:二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素
(2)根据题目中的信息,高锰酸钾溶液遇到二氧化硫会褪色,故上图C装置的作用是:验证二氧化硫是否除干净,以免对后面二氧化碳存在的判断形成干扰
(3)根据质量守恒定律:化学反应前后,元素的种类不变,故要证明煤中含有碳元素和硫元素的现象是:B中的溶液褪色,说明煤粉燃烧产生二氧化硫,从而证明煤粉中含有硫元素,C中的溶液不褪色,说明二氧化硫全部除尽,D中澄清的石灰水变浑浊,说明燃烧生成二氧化碳,从而证明煤粉中含有碳元素

【题目】实验室中有一瓶久置的氢氧化钠溶液,以下实验设计合理的是
序号 | 实验目的 | 实验操作 |
① | 证明溶液发生变质 | 取少量溶液,加入足量稀盐酸 |
② | 确定溶液中溶质的成分 | 取少量溶液,加入适量氢氧化钡溶液,过滤,向滤液中滴加酚酞溶液 |
③ | 测定溶液中碳酸钠的质量分数 | 取一定质量溶液,加入足量稀盐酸,将生成的气体通入浓硫酸,测浓硫酸的增重 |
④ | 除去溶液中的碳酸钠 | 向溶液中滴加氢氧化钡溶液至恰好完全反应,过滤 |
A.①② B.②③ C.①④ D. ②④
【题目】下列除去杂质的方法中,合理的是
选项 | 物质 | 杂质 | 除杂方法 |
A | CO2 | 水蒸气 | 通入浓硫酸中 |
B | NaCl溶液 | NaOH溶液 | 加入适量BaCl2溶液,过滤 |
C | 铁粉 | 铜粉 | 加入足量的稀硫酸,过滤 |
D | CaO | CaCO3 | 加入适量稀盐酸,过滤 |