题目内容
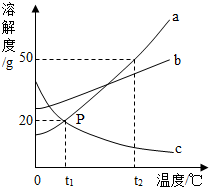 请根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
请根据图中a、b、c三种物质的溶解度曲线,回答下列问题:(1)P点的含义是
(2)t2℃时,30g a物质加入到50g水中不断搅拌,能形成80g溶液吗?
(3)将t2℃时的a、b、c三种物质的饱和溶液降温到t1℃时,溶液中溶质质量分数最小的是
(4)现有a、b、c三种物质的浓溶液,适用于海水晒盐原理进行结晶的是
分析:(1)两条溶解度曲线的交点,表示在该点所示的温度下,两种物质的溶解度相等;
(2)根据溶解度曲线可以查找指定温度时物质的溶解度,利用图示的曲线,查出t2℃时物质a的溶解度,判断将30g物质a放入50g水中是否可以完全溶解;
(3)根据溶解度曲线可以比较和确定物质的溶解度受温度影响的程度,利用图示的曲线,判断a、b、c三种物质的溶解度随温度降低而改变情况,并利用饱和溶液的质量分数=
×100%,判断三种物质t2℃时的饱和溶液降温到t1℃时溶质质量分数大小;
(4)海水晒盐原理是蒸发溶剂水而析出晶体,此方法适应于溶解度受温度影响不大的物质的结晶.
(2)根据溶解度曲线可以查找指定温度时物质的溶解度,利用图示的曲线,查出t2℃时物质a的溶解度,判断将30g物质a放入50g水中是否可以完全溶解;
(3)根据溶解度曲线可以比较和确定物质的溶解度受温度影响的程度,利用图示的曲线,判断a、b、c三种物质的溶解度随温度降低而改变情况,并利用饱和溶液的质量分数=
| 溶解度 |
| 100+溶解度 |
(4)海水晒盐原理是蒸发溶剂水而析出晶体,此方法适应于溶解度受温度影响不大的物质的结晶.
解答:解:(1)P点为t1℃时a、c两种物质的溶解度曲线的交点,表明t1℃时a、c两种物质的溶解度相等;
(2)由图示的a物质的溶解度曲线,可知t2℃时物质a的溶解度为50g,即此时100g水最多可溶解a物质50g,因此,t2℃时50g水中最多只能溶解a物质25g;所以,30g a物质加入到50g水中不断搅拌,在t2℃时只能形成50g+25g=75g的溶液而不能形成80g溶液;
(3)由a、b、c三种物质的溶解度曲线可知,a、b两物质的溶解度随温度降低而减小,c物质的溶解度随温度降低而增大,因此,将t2℃时的a、b、c三种物质的饱和溶液降温到t1℃时,a、b两物质的饱和溶液中析出晶体后变成t1℃时的饱和溶液,物质c的饱和溶液变成了不饱和溶液而其溶液的溶质质量分数不变;t1℃时a、b两物质的溶解度大于t2℃时c物质的溶解度,利用饱和溶液的质量分数=
×100%,可判断三种物质t1℃时溶质质量分数最小的为c物质的不饱和溶液;
(4)由图示的三种物质的溶解度曲线可知,物质a的溶解度随温度升高而增大,曲线为“陡升型”,溶解度受温度影响大;物质b的溶解度受温度的影响很小,曲线为“缓升型”;物质c的溶解度随温度的升高而减小,曲线为“下降型”;其中适用于海水晒盐原理进行结晶的是溶解度受温度影响不大物质b;
故答案为:(1)t1℃时a、c两种物质的溶解度相等;
(2)不能;
(3)c;
(4)b.
(2)由图示的a物质的溶解度曲线,可知t2℃时物质a的溶解度为50g,即此时100g水最多可溶解a物质50g,因此,t2℃时50g水中最多只能溶解a物质25g;所以,30g a物质加入到50g水中不断搅拌,在t2℃时只能形成50g+25g=75g的溶液而不能形成80g溶液;
(3)由a、b、c三种物质的溶解度曲线可知,a、b两物质的溶解度随温度降低而减小,c物质的溶解度随温度降低而增大,因此,将t2℃时的a、b、c三种物质的饱和溶液降温到t1℃时,a、b两物质的饱和溶液中析出晶体后变成t1℃时的饱和溶液,物质c的饱和溶液变成了不饱和溶液而其溶液的溶质质量分数不变;t1℃时a、b两物质的溶解度大于t2℃时c物质的溶解度,利用饱和溶液的质量分数=
| 溶解度 |
| 100+溶解度 |
(4)由图示的三种物质的溶解度曲线可知,物质a的溶解度随温度升高而增大,曲线为“陡升型”,溶解度受温度影响大;物质b的溶解度受温度的影响很小,曲线为“缓升型”;物质c的溶解度随温度的升高而减小,曲线为“下降型”;其中适用于海水晒盐原理进行结晶的是溶解度受温度影响不大物质b;
故答案为:(1)t1℃时a、c两种物质的溶解度相等;
(2)不能;
(3)c;
(4)b.
点评:根据溶解度曲线,可以看出物质的溶解度随着温度的变化而变化的情况,可以比较在一定温度范围内的物质的溶解度大小,可以判断某温度下物质的溶解度.

练习册系列答案
相关题目
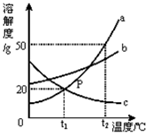 请根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
请根据图中a、b、c三种物质的溶解度曲线,回答下列问题: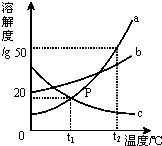 请根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
请根据图中a、b、c三种物质的溶解度曲线,回答下列问题: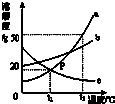 请根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
请根据图中a、b、c三种物质的溶解度曲线,回答下列问题: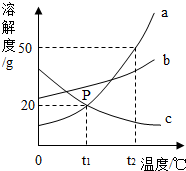 请根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
请根据图中a、b、c三种物质的溶解度曲线,回答下列问题: