题目内容
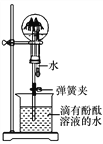
【题目】利用如图装置探究物质的性质(部分固定装置略)。
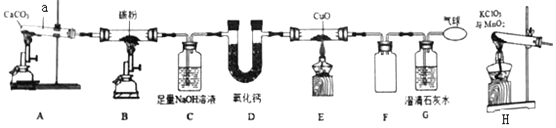
①仪器a的名称_____;装置A中反应的化学方程式_____;
②装置C 的作用_____; 装置D中反应的化学方程式为_____;
③装置E中固体由黑色变成亮红色,反应化学方程式为_____;
④装置F是安全瓶,其作用是_____;
⑤把装置A中换成酒精灯,可用于氯酸钾与二氧化锰混合制取氧气。试管中固体的质量随反应时间变化的数据见如表。
反应时间/min | 0 | t1 | t2 | t3 |
固体质量/g | 26.0 | 20.2 | 16.4 | 16.4 |
Ⅰ.共制得氧气的质量是_____g;
Ⅱ.参加反应的氯酸钾的物质的量是_____mol(通过化学方程式列式计算)
【答案】 试管 ; CaCO3![]() CaO+CO2↑ ; 除去混合气中额二氧化碳 ; CaO+H2O=Ca(OH)2 ; CuO+CO
CaO+CO2↑ ; 除去混合气中额二氧化碳 ; CaO+H2O=Ca(OH)2 ; CuO+CO![]() Cu+CO2 ; 防止澄清石灰水倒流,炸裂玻璃管 ; 9.6 g; 0.2 mol
Cu+CO2 ; 防止澄清石灰水倒流,炸裂玻璃管 ; 9.6 g; 0.2 mol
【解析】①仪器a的名称是试管;碳酸钙在高温的条件下煅烧分解生成二氧化碳和氧化钙,反应方程式为CaCO3![]() CaO+CO2↑;
CaO+CO2↑;
②装置E中是用一氧化碳还原氧化铜的实验,为了不影响该实验,故要用足量的氢氧化钠将混合气体中的二氧化碳除尽,故装置C 的作用是除尽混合气体中的二氧化碳气体;装置D中是氧化钙与水反应生成氢氧化钙,反应方程式为CaO+H2O=Ca(OH)2;
③装置E中是氧化铜与一氧化碳反应生成铜和二氧化碳,反应方程式为CuO+CO![]() Cu+CO2;
Cu+CO2;
④装置F的作用是防止澄清石灰水倒流,炸裂玻璃管;
⑤Ⅰ.由表可知,反应前各物质的总质量为26.0g,反应后剩余物质的质量为16.4g,故生成氧气的质量为26.0g-16.4g=9.6g;
Ⅱ.设参加反应的氯酸钾的物质的量是xmol
2KClO3![]() 2KCl + 3O2↑
2KCl + 3O2↑
2 96
X 9.6g
![]() =
=![]() 解得x=0.2mol
解得x=0.2mol

 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案