��Ŀ����
����Ŀ��ʵ�����ü�ʽ̼��ͭ[��ѧʽ��Cu2��OH��2CO3]�Ʊ�����ͭ����������װ�����£� 
����һ������A��B��������ͨ�������
��������رջ���������C��D����ʼ���ȣ�
���������ڼ��ȹ����У���¼B�й��������仯���±�����t3ʱֹͣ���ȣ�
����ʱ�䣨min�� | 0 | t1 | t2 | t3 |
B���������g�� | 6.66 | 5.20 | 4.80 | 4.80 |
��1������һͨ�������Ŀ���� ��
��2��C���Լ����������ƣ���A�����������տ����е��������ƣ���
��3��ѡ��t3ʱֹͣ���ȵ������� ��
��4��B�з�����Ӧ�Ļ�ѧ����ʽΪ�� ��
���𰸡�
��1���ų�Ӳ�ʲ�����B�е�ˮ�����Ͷ�����̼����ֹ����ʵ����
��2����ˮ����ͭ��ˮ�����Ͷ�����̼
��3��t3ʱ��t2ʱ��ȣ������������ٸı䣬˵����ʽ̼��ͭ����ȫ�ֽ�
��4��Cu2��OH��2CO3 ![]() 2CuO+H2O+CO2��
2CuO+H2O+CO2��
���������⣺��1��װ���ں��еĿ����е�ˮ�����Ͷ�����̼��ʵ���������Ӱ�죬���Բ���һͨ�������Ŀ���ǣ��ų�Ӳ�ʲ�����B�е�ˮ�����Ͷ�����̼����ֹ����ʵ��������2����ˮ����ͭ��ˮ����ɫ���ռ�����ˮ�Ժͳ�����������еĶ�����̼��Ӧ�����Լ���ˮ������ˮ����ͭ�����������̼���ó���ʯ��ˮ����Ҫ�ȼ���ˮ���ټ��������̼������C���Լ�����ˮ����ͭ�������еĶ�����̼��ˮ������Զ�����̼��ˮ�����ļ�����ɸ��ţ�����A�ռ��������������տ����еĶ�����̼��ˮ��������3�������������ٱ仯ʱ��������Ϊ��ʽ̼��ͭ��ȫ�ֽ⣬t2 �� t3ʱ�����������ٸı䣬����ѡ��t3ʱֹͣ���ȵ������ǣ������������ټ��٣�֤����ʽ̼��ͭ�Ѿ���ȫ�ֽ⣻��4����ʽ̼��ͭ�ڼ��ȵ���������������ͭ��ˮ�Ͷ�����̼����ѧ����ʽΪ��Cu2��OH��2CO3 ![]() 2CuO+H2O+CO2���� ���Դ��ǣ���1���ų�Ӳ�ʲ�����B�е�ˮ�����Ͷ�����̼����ֹ����ʵ������2����ˮ����ͭ��ˮ��������3��t3ʱ��t2ʱ��ȣ������������ٸı䣬˵����ʽ̼��ͭ����ȫ�ֽ⣻��4��Cu2��OH��2CO3
2CuO+H2O+CO2���� ���Դ��ǣ���1���ų�Ӳ�ʲ�����B�е�ˮ�����Ͷ�����̼����ֹ����ʵ������2����ˮ����ͭ��ˮ��������3��t3ʱ��t2ʱ��ȣ������������ٸı䣬˵����ʽ̼��ͭ����ȫ�ֽ⣻��4��Cu2��OH��2CO3 ![]() 2CuO+H2O+CO2����
2CuO+H2O+CO2����
�����㾫����������Ĺؼ�����������д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ�����֪ʶ������ע�⣺a����ƽ b������ c�����ţ�

 ���ٴ�����ɽ����ϵ�д�
���ٴ�����ɽ����ϵ�д�����Ŀ��Ϊ̽��Ӱ��˫��ˮ�ֽ��ٶȵ�ij�����أ���¼������ʵ�����ݣ�
˫��ˮ������ | ˫��ˮ��Ũ�� | MnO2������ | ��ͬʱ���ڲ���O2����� | |
�� | 50.0g | 1% | 0.1g | 9mL |
�� | 50.0g | 2% | 0.1g | 16mL |
�� | 50.0g | 4% | 0.1g | 31mL |
�����ݴ��������ۡ�
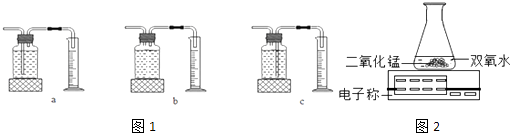
��1����ʵ���У�����O2�����װ������ѡ��ͼ1�е�װ�ñ�ţ���
��2��ʵ����ۣ�����ͬ�����£� �� ˫��ˮ�ֽ�����Խ�죮
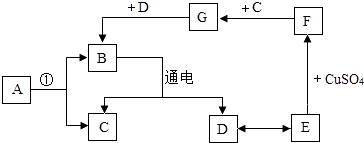
��3��CС������ͼ2װ�ý���ʵ�飬ͨ���Ƚ�Ҳ�ܴﵽʵ��Ŀ�ģ�