题目内容
【题目】金属是一类重要的材料,研究其性质十分必要。
(1)人们对铝的利用比铜和铁晚。金属的发现和利用的先后顺序主要与_______(填序号)有关。
A.金属的活动性 B.金属的导电性 C.金属的导热性
(2)“真金不怕火炼”说明金的___________________;鉴别黄金和黄铜(铜、锌合金)可以使用的方法:①_________________________; ②______________________。
(3)下面是某小组同学对金属镁和铁性质的对比研究。
①在室温条件下进行如图所示实验。试管内的镁和铁表面均被打磨过,且形状、大小均相同,向两支试管中同时加入相同质量的稀盐酸。可观察到单位时间内产生气泡多的是______(填“镁”或“铁”),可得出的结论是:金属活动性______>_______(填元素符号)。
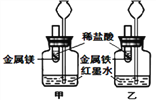
②已知化学反应一般伴随着能量变化,因此,还可以观察到反应在相同时间内,两支长颈漏斗内的液面高度不同,长颈漏斗内液面上升较高的是_______(填“镁”或“铁”,下同),由此可得出的结论是:在单位时间内,等质量的镁、铁分别与等质量的盐酸反应放出的热量多的是________。
【答案】 A 化学性质不活泼(或稳定) 加热观察表面是否变黑 或加入稀硫酸观察表面是否产生气泡或加入硝酸银溶液观察表面是否出现银白色固体 镁 Mg Fe 镁 镁
【解析】 (1) 人们对铝的利用比铜和铁晚.金属大规模开发和利用的先后顺序与金属的活动性有关,活动性越强,发现的越晚;(2)“真金不怕火炼”说明金的化学性质稳定,即使高温条件下也不与氧气反应;鉴别黄金和黄铜(铜、锌合金)可以使用的方法:①灼烧:黄金不变色,黄铜中的铜会因生成氧化铜而变黑,而金无明显变化; ②分别取少量样品放入适量的盐酸中,黄铜中含有锌,能与酸反应生成气体,而冒气泡,而金不能;加入硝酸银溶液,锌和铜的的活动性比银的强,观察表面出现银白色固体,而金没有;(3)①金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au,在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的活动性越强,反应也越快。试管内的镁和铁表面均被打磨过,且形状、大小均相同,向两支试管中同时加入相同质量的稀盐酸。可观察到单位时间内产生气泡多的是镁,由此得出的结论是:金属活动性:Mg > Fe;②反应放热使瓶内气体压强增大,液体进入漏斗内,使漏斗内液面升高,放热越多,升高越明显,观察到反应在相同时间内,长颈漏斗内液面上升较高的是镁,由此可得出的结论是:在单位时间内,等质量的镁、铁分别与等质量的盐酸反应放出的热量多的是镁。

 口算能手系列答案
口算能手系列答案