题目内容
 等质量的甲、乙两种金属,分别与相同质量分数的足量盐酸反应(已知甲、乙在反应中均显+2价),生成氢气的质量和反应时间的关系如图所示,下列叙述正确的是( )
等质量的甲、乙两种金属,分别与相同质量分数的足量盐酸反应(已知甲、乙在反应中均显+2价),生成氢气的质量和反应时间的关系如图所示,下列叙述正确的是( )| A、甲、乙两种金属中较活泼的是乙 | B、相对原子质量较大的是乙 | C、生成氢气的质量甲<乙 | D、产生氢气的速率甲<乙 |
练习册系列答案
相关题目
制印刷电路时,常用氯化铁溶液作为腐蚀液,将铜腐蚀掉.其反应方程式为:FeCl3+Cu→2FeCl2+CuCl2.现向氯化铁溶液中加入ag铜,完全溶解后,再加入bg铁,充分反应后得到cg残余固体,且a>c.则下列说法正确的是( )
| A、c g残余固体全部是铜 | B、c g残余固体可能为铁和铜的混合物 | C、最后得到的溶液中可能含有+3价Fe元素 | D、溶液中一定不含Cu元素 |
将过量的铁粉加入Cu(N03)2和AgN03的混合溶液中,充分反应后过滤,下列对滤渣和滤液的说明中,不正确的是( )
| A、滤渣中一定含有银 | B、向滤渣中滴入稀盐酸,有气泡放出 | C、滤液可能为蓝色 | D、向滤液中滴入稀盐酸,无明显现象 |
把一定量的铁粉加入Cu(NO3)2和AgNO3的混合溶液中,反应结束后过滤,向滤渣中加入稀盐酸,无明显现象,下列对滤液和滤渣的说法错误的是( )
| A、滤渣中一定含有银 | B、滤液中一 定含有Fe2+ | C、滤渣中可能含有铜 | D、滤液中一定含有Cu2+ |
将一定质量的Zn粒放入AgNO3与Cu(NO3)2的混合溶液中,充分反应后发现,溶液底部有少量固体;过滤后在滤渣和滤液中分别加入适量稀盐酸,滤渣中有无色气体产生,滤液中无沉淀产生.结合实验现象判断,下列结论中,正确的是( )
| A、滤渣中可能含有单质锌 | B、滤液中一定没有银离子 | C、滤渣中一定没有单质铜 | D、滤液的颜色可能为蓝色 |
下列图象与对应的叙述相符合的是( )
A、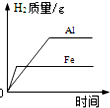 等质量的铁片、铝片分别与足量且质量分数相同的稀硫酸反应 | B、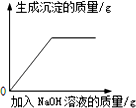 向一定量的H2SO4和CuSO4的混合溶液中滴加NaOH溶液 | C、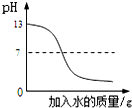 向pH=13的氢氧化钠溶液中不断加水稀释 | D、 向接近饱和的硝酸钾溶液中加入硝酸钾固体 |
 X、Y、Z三种金属的活动性依次增强,且都比Mg弱.现进行如图所示的甲、乙两个实验.下列叙述正确的是( )
X、Y、Z三种金属的活动性依次增强,且都比Mg弱.现进行如图所示的甲、乙两个实验.下列叙述正确的是( )| A、实验甲中,溶液的颜色一定会发生变化 | B、实验乙中,金属Y表面一定有气体产生 | C、实验甲中,金属Y渐渐被消耗掉部分或全部 | D、实验乙中,若Y被消耗了,则溶液一定会出现别的颜色 |
根据金属活动性顺序Fe>Cu>Ag判断,下列说法错误的是( )
| A、反应Cu+FeSO4═Fe+CuSO4可以发生 | B、反应Fe+2AgNO3═2Ag+Fe(NO3)2可以发生 | C、铜片放入硝酸银溶液中,颜色由无色变成蓝色 | D、铁丝插入硫酸铜溶液中,铁丝表面有红色物质析出 |
