题目内容
【题目】将含有硫酸的硫酸镁溶液转变为中性溶液,在没有任何指示剂的条件下,可选用:
A. NaOH B. Mg
C. Ba(OH)2 D. BaCl2
【答案】B
【解析】氢氧化钠和硫酸反应无明显现象,易导致过量,使溶液呈碱性;镁与硫酸反应生成硫酸镁和氢气,得硫酸镁溶液;氢氧化钡和硫酸、硫酸铜都反应最终得到的是硫酸钡沉淀、氢氧化镁沉淀、水;氯化钡和硫酸、硫酸镁溶液都反应,最终得到的是硫酸钡和盐酸,溶液呈酸性;选B

【题目】下表列出了除去物质中所含少量杂质的方法,其中不正确的是
选项 | 物质 | 所含杂质 | 除去杂质的方法 |
A | CaO | CaCO3 | 加水溶解、过滤 |
B | N2 | O2 | 将气体缓缓通过足量的灼热铜网 |
C | FeCl2 | CuCl2 | 加入过量的锌粉,过滤 |
D | Cu | Zn | 加入过量的稀盐酸,过滤,洗涤,干燥 |
A. A B. B C. C D. D
【题目】下列是关于溶液的一些图表和图像,请根据图示回答问题:

(1)甲、乙两种固体的物质的溶解度曲线如图1所示,分析并回答下列问题。
①溶解度随温度升高而减小的物质是_____;
②20℃时,将等质量的甲、乙分别加入盛有等质量水的试管中,充分溶解后如图2所示。据此推断,图1中![]() ℃___20℃(填“>”、“<”或“=”);
℃___20℃(填“>”、“<”或“=”);
(2)某烧杯中盛有60℃一定质量的甲溶液,将其置于室温环境中,测定不同温度时析出固体甲的质量。测定结果记录如下表。
溶液的温度/℃ | 55 | 50 | 40 | 30 | 20 |
析出固体甲的质量/ | 0 | 0 | 2.0 | 4.5 | 8.4 |
若不考虑水蒸发对实验的影响,请思考:50℃时,该溶液是否为饱和溶液?_______(填“是”、“否”或“无法判断”);
(3)小强同学要在实验室配制15%的氯化钠溶液50g,请在图的标签中填上相应的内容。_______
【题目】在学习盐酸的化学性质时,小红、芳芳两位同学分别作了碳酸钠溶液和稀盐酸反应的实验如图所示。

【实验现象】小红在实验中观察到有气泡冒出,而芳芳
所做的实验无现象。写出小红实验的化学反应方程式:________________。
【实验讨论】芳芳同学的试验为什么观察不到有气泡?
反应后溶液的溶质有哪些?
【查阅资料】①碳酸钠和稀盐酸反应生成物受到盐酸的质
量影响,稀盐酸过量生成二氧化碳,若盐酸量不足则生成碳酸氢钠;②碳酸氢钠与氯化钙溶液混合不发生反应,而碳酸钠和氯化钙溶液反应生成沉淀,且碳酸钠和碳酸氢钠溶液都呈碱性,氯化钙溶液呈中性。
【猜想与假设】实验反应后溶液中溶质可能有:①NaHCO3、NaCl、Na2CO3; ②NaHCO3、NaCl;
③NaHCO3、NaCl、HCl。
芳芳同学认为猜想③肯定不成立,理由是______________。
【实验设计】确定芳芳同学实验是否生成碳酸氢钠,并证明反应后的产物。
实验步骤 | 实验现象 | 实验结论 |
A、取上述溶液少量于试管中,加 入足量的________溶液。 | 产生白色沉淀 | 猜想①正确 |
B、取步骤A所得上层清液少量,滴加_______溶液。 | ___________ |
【实验反思】若用少量的稀盐酸鉴定氢氧化钠是否变质,发现无气泡冒出,则证明氢氧化钠溶液没有变质。对此实验结论,你是否赞同?若不赞同,还需说明理由。_____________。
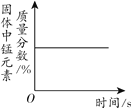
【题目】下列4个图像中,能正确反映对应变化关系的是
|
|
|
|
A.向一定质量的碳酸钙粉末中加入稀盐酸至过量 | B.向少量的稀硫酸中加入锌片 | C.加热一定质量的高锰酸钾固体 | D.向一定质量的二氧化锰中加入过氧化氢溶液 |
A. A B. B C. C D. D