题目内容
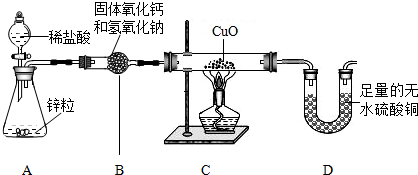
硫酸中氢元素的质量分数为________;若要将10g98%的浓硫酸稀释成19.6%的稀硫酸,应将这10g98%的浓硫酸加入到________ g水中.
分析:硫酸中氢元素的质量分数为:
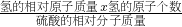 ×100;
×100;根据溶液稀释前后溶质的质量不变和“溶质质量=溶液质量×溶质质量分数”计算.
解答:硫酸中氢元素的质量分数:
 ×100%═2.04%,
×100%═2.04%,溶液稀释前后溶质的质量不变,可设应将浓硫酸加入到水的质量为X,则可得出
10×98%═(10+X)×19.6%
则X═40g
故答案为:2.04%;40
点评:本题主要是运用化学式进行计算的问题.解题时要注意稀释溶液前后溶质的质量不变.

 黄冈创优卷系列答案
黄冈创优卷系列答案(14分)(1)实验室中常用氯酸钾和二氧化锰加热制氧气、锌粒与稀硫酸反应制氢气、石灰石与稀盐酸制二氧化碳气体。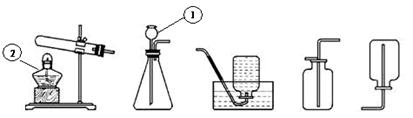
A B C D E
(1)写出标号仪器的名称① ②
请结合所给药品选择适当的气体发生和收集装置填入下表:(填字母)
| 制取的气体 | 发生装置 | 收集装置 |
| O2 | | |
| H2 | | |
| CO2 | | |
(2)写出实验室用石灰石与稀盐酸制二氧化碳气体的化学方程式:
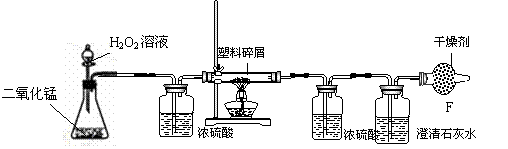
(3)由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题。某化学研究小组的同学欲对某种塑料袋的组成进行分析探究(资料显示该塑料只含C、H两种元素),他们设计了如图所示的实验装置,使该塑料试样在纯氧中燃烧,观察实验现象,分析有关数据,推算元素含量。
A B C D E
①仪器B的作用是 。
②仪器E中的现象是 。
③若仪器C的玻璃管中放入的塑料试样质量为W g,塑料试样充分燃烧后,若仪器D增重a g,则W g该塑料试样中含氢元素的质量为 g(计算结果可为分数形式)
④若装置中没有连接仪器B,将使该塑料试样中氢元素的质量测算结果
(填“偏小”、“偏大”、“无影响”中之一)。
(14分)(1)实验室中常用氯酸钾和二氧化锰加热制氧气、锌粒与稀硫酸反应制氢气、石灰石与稀盐酸制二氧化碳气体。

A B C D E
(1)写出标号仪器的名称 ① ②
请结合所给药品选择适当的气体发生和收集装置填入下表:(填字母)
|
制取的气体 |
发生装置 |
收集装置 |
|
O2 |
|
|
|
H2 |
|
|
|
CO2 |
|
|
(2)写出实验室用石灰石与稀盐酸制二氧化碳气体的化学方程式:
(3)由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题。某化学研究小组的同学欲对某种塑料袋的组成进行分析探究(资料显示该塑料只含C、H两种元素),他们设计了如图所示的实验装置,使该塑料试样在纯氧中燃烧,观察实验现象,分析有关数据,推算元素含量。

A B C D E
①仪器B的作用是 。
②仪器E中的现象是 。
③若仪器C的玻璃管中放入的塑料试样质量为W g,塑料试样充分燃烧后,若仪器D增重a g,则W g该塑料试样中含氢元素的质量为 g(计算结果可为分数形式)
④若装置中没有连接仪器B,将使该塑料试样中氢元素的质量测算结果
(填“偏小”、“偏大”、“无影响”中之一)。
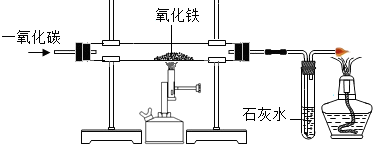 铁、铝、铜是日常生活中使用最广泛的金属.
铁、铝、铜是日常生活中使用最广泛的金属. (2012?绍兴)21世纪是海洋开发与利用的世纪.
(2012?绍兴)21世纪是海洋开发与利用的世纪.