题目内容
【题目】某粗盐样品中含有杂质氯化镁、氯化钙.某同学设计了以下提纯方案: 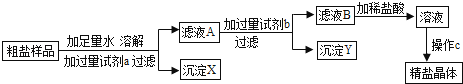
请回答下列问题:
(1)方案中加入过量试剂a若为氢氧化钠溶液,则其目的是为了除去粗盐中的 .
(2)在过滤操作中,除用到带铁圈的铁架台、烧杯、玻璃棒外,还需要用到的仪器是 .
(3)滤液B中所含的溶质为 .
(4)向滤液B滴加稀盐酸的过程中,当观察到的溶液的现象为时,应停止滴加,如果滴加的稀盐酸过量,对最后得到的精盐晶体的成分(填“有”或“没有”)影响.
(5)操作C的名称为 .
(6)工业上用电解饱和食盐水的方法可制取氢氧化钠、氢气、和氯气,写出反应的化学方程式 .
【答案】
(1)氯化镁
(2)漏斗
(3)氯化钠、氢氧化钠,碳酸钠
(4)无气泡放出;没有
(5)蒸发
(6)2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
【解析】解:(1)因为钠盐都溶于水,而氢氧根离子会将镁离子转化为氢氧化镁沉淀,剩余氯化钠.所以答案是:氯化镁.(2)过滤实验中要用到的仪器有:漏斗、铁架台、烧杯、玻璃棒.
所以答案是:漏斗.(3)前面的除杂各步后都剩下氯化钠,但是在除杂时加入的氢氧化钠和碳酸钠(除去氯化钙时,用过量的碳酸钠,即过量的试剂b)都是过量的.所以答案是:氯化钠、氢氧化钠,碳酸钠.(4)向滤液B滴加稀盐酸的过程中,当观察到溶液中不产生气泡时,说明恰好完全反应,停止滴加;过量的稀盐酸对最后得到的精盐晶体的成分没有影响,因为稀盐酸不与氯化钠反应;所以答案是:无气泡放出;没有.(5)得到精盐晶体之前的操作是蒸发.
所以答案是:蒸发.(6)由分析可知,反应物、生成物、反应条件;故可书写此化学方程式为:2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑故答为:2NaCl+2H2O
2NaOH+Cl2↑+H2↑故答为:2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑.
2NaOH+Cl2↑+H2↑.
【考点精析】本题主要考查了过滤操作的注意事项的相关知识点,需要掌握过滤操作注意事项:“一贴”“二低”“三靠;过滤后,滤液仍然浑浊的可能原因有:①承接滤液的烧杯不干净②倾倒液体时液面高于滤纸边缘③滤纸破损才能正确解答此题.