题目内容
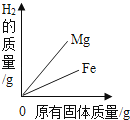
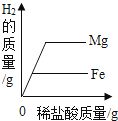
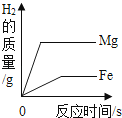
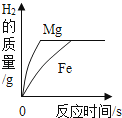
【题目】向等质量的相同的稀硫酸中分别加入足量的镁条、铁片、锌粒,有关量的关系图象如下,其中正确的是( )
A.
B.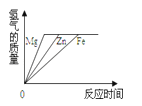
C.
D.
【答案】B
【解析】金属活动性顺序可知,三种金属镁最活泼,锌次之,铁最不活泼,所以镁与稀硫酸反应速率最快,锌次之,铁反应最慢,向等质量的相同的稀硫酸中分别加入足量的镁条、铁片、锌粒,金属是足量的,所以生成氢气的质量相等,通过分析可知,故选:B.
【考点精析】根据题目的已知条件,利用金属材料的选择依据和金属活动性顺序及其应用的相关知识可以得到问题的答案,需要掌握黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属;在金属活动性顺序里:1、金属的位置越靠前,它的活动性就越强2、位于氢前面的金属能置换出盐酸、稀硫酸中的氢(不可用浓硫酸、硝酸)3、位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来.(除K、Ca、Na).

练习册系列答案
相关题目