题目内容
(2013?广陵区一模)材料化学无处不在.
(1)图1中,无机材料是
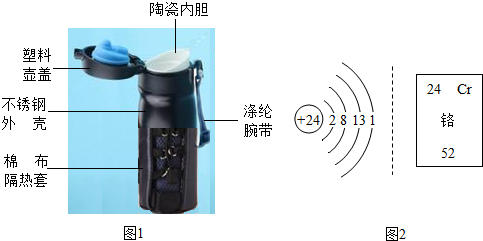
a.不锈钢外壳 b.棉布隔热套 c.塑料壶盖 d.陶瓷内胆 e.涤纶腕带
(2)涤纶的基本组成物质是聚酯纤维[(H8C6O5N)n],由
(3)钢是含碳量
(4)不锈钢的耐腐蚀性主要取决于铬(Cr)元素.在450~850℃时,Cr和C反应生成的Cr23C6会降低不锈钢的耐腐蚀性,反应的化学方程式为
(5)图2是Cr原子结构示意图及其在元素周期表的信息,下列说法正确的是
A.铬原子中,中子数是24
B.铬原子的相对质量是52g
C.铬原子在化学变化中易失去电子
D.铬元素是一种非金属元素.
(1)图1中,无机材料是
d
d
,合成材料是ce
ce
,天然材料是b
b
;
a.不锈钢外壳 b.棉布隔热套 c.塑料壶盖 d.陶瓷内胆 e.涤纶腕带
(2)涤纶的基本组成物质是聚酯纤维[(H8C6O5N)n],由
4
4
种元素组成,C元素的质量分数约为41.4%
41.4%
.棉布是由纤维素[(C6H10O5)n]制成,鉴别涤纶和棉布的简易方法是灼烧,闻气味
灼烧,闻气味
;(3)钢是含碳量
<
<
(填“>”或“=”或“<”)生铁,成语“百炼成钢”是指灼热的生铁经反复捶打转变为钢的过程,其中反应的化学方程式为C+O2
CO2
| ||
C+O2
CO2
;
| ||
(4)不锈钢的耐腐蚀性主要取决于铬(Cr)元素.在450~850℃时,Cr和C反应生成的Cr23C6会降低不锈钢的耐腐蚀性,反应的化学方程式为
23Cr+6C
Cr23C6
| ||
23Cr+6C
Cr23C6
;
| ||
(5)图2是Cr原子结构示意图及其在元素周期表的信息,下列说法正确的是
C
C
;A.铬原子中,中子数是24
B.铬原子的相对质量是52g
C.铬原子在化学变化中易失去电子
D.铬元素是一种非金属元素.
分析:(1)根据陶瓷属于无机材料、塑料和涤纶属于合成材料、棉布属于天然材料,而不锈钢属于金属材料进行解答;
(2)根据聚酯纤维的化学式为[(H8C6O5N)n]可知其元素组成、碳元素的质量分数以及涤纶和棉布燃烧会产生不同的气味进行解答;
(3)根据钢的含碳量小于生铁的含碳量以及碳燃烧生成二氧化碳进行解答;
(4)根据Cr和C在加热条件下反应生成的Cr23C6进行解答;
(5)根据元素周期表中提供的信息进行解答.
(2)根据聚酯纤维的化学式为[(H8C6O5N)n]可知其元素组成、碳元素的质量分数以及涤纶和棉布燃烧会产生不同的气味进行解答;
(3)根据钢的含碳量小于生铁的含碳量以及碳燃烧生成二氧化碳进行解答;
(4)根据Cr和C在加热条件下反应生成的Cr23C6进行解答;
(5)根据元素周期表中提供的信息进行解答.
解答:解:(1)陶瓷属于无机材料、塑料和涤纶属于合成材料、棉布属于天然材料,而不锈钢属于金属材料;
(2)由聚酯纤维的化学式为[(H8C6O5N)n]可知其元素组成为碳、氢、氧、氮四种元素;碳元素的质量分数=
×100%=41.4%,涤纶和棉布燃烧会产生不同的气味,所以鉴别涤纶和棉布的简易方法是灼烧,闻气味;
(3)钢的含碳量小于生铁的含碳量;成语“百炼成钢”是指灼热的生铁经反复捶打转变为钢的过程,就是将碳高温生成二氧化碳,其中反应的化学方程式为C+O2
CO2;
(4)Cr和C在加热条件下反应生成的Cr23C6,反应的化学方程式为23Cr+6C
Cr23C6;
(5)根据元素周期表中提供的信息可知铬原子中,中子数=52-24=28;铬原子的相对质量是52g;铬原子在化学变化中易失去电子;铬元素是一种金属元素.
故答案为:
(1)d;ce;b;(2)4;41.4%;灼烧,闻气味;(3)<;C+O2
CO2;(4)23Cr+6C
Cr23C6;(5)C.
(2)由聚酯纤维的化学式为[(H8C6O5N)n]可知其元素组成为碳、氢、氧、氮四种元素;碳元素的质量分数=
| 12×6×n |
| (1×8+12×6+16×5+14)×n |
(3)钢的含碳量小于生铁的含碳量;成语“百炼成钢”是指灼热的生铁经反复捶打转变为钢的过程,就是将碳高温生成二氧化碳,其中反应的化学方程式为C+O2
| ||
(4)Cr和C在加热条件下反应生成的Cr23C6,反应的化学方程式为23Cr+6C
| ||
(5)根据元素周期表中提供的信息可知铬原子中,中子数=52-24=28;铬原子的相对质量是52g;铬原子在化学变化中易失去电子;铬元素是一种金属元素.
故答案为:
(1)d;ce;b;(2)4;41.4%;灼烧,闻气味;(3)<;C+O2
| ||
| ||
点评:主要考查了生活中常见的几种材料、元素周期表等方面的知识和化学方程式的书写,培养学生分析问题、解决问题的能力,难度稍大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 (2013?广陵区一模)如图为甲乙两物质的溶解度曲线,下列说法不正确的是( )
(2013?广陵区一模)如图为甲乙两物质的溶解度曲线,下列说法不正确的是( )