题目内容
生产、生活、科技、环保等都离不开化学。
Ⅰ.食品、药物安全一直是人们关注的话题。
⑴2012年4月17日经央视新闻频道曝光的用工业明胶制成的医用“毒胶囊”震惊全国。据悉,其中混有的重金属铬对人体有害。这里的铬是指 (填“元素”或“单质”或“元素”)。
⑵我市盛产的海产品鱼虾中富含基本营养素(糖类、油脂、蛋白质、维生素)中的 。
Ⅱ.材料的应用与发展,大大方便了人们的生活。请用下列三种材料的对应字母填空。
A.有机合成材料 B.金属材料 C.天然有机高分子材料 D、无机非金属材料
⑴塑料制品属于 。
⑵蚕丝、羊毛、棉花属于 。
⑶可用于制造人造骨、航天飞机等的钛合金属于 。
Ⅲ.随着人们生活水平的提高,私家车拥有量越来越多,酒驾会对人和社会造成非常不良的后果。
啤酒、红酒和白酒中都含有乙醇(C2H5OH),饮酒后乙醇可进入人体血液中,科学实验表明,当乙醇在人体血液中的含量超过80mg /100mL血(每100mL血中含有80mg乙醇)时,便会影响人的驾车或操作机器的能力;已知饮用某啤酒1大杯(0.56L),会使血液中乙醇含量升高30mg/100mL血。回答下列问题:
(1)乙醇分子中碳、氢、氧原子个数比是 。写出乙醇燃烧的化学方程式 。
(2)李明饮用了3大杯上述啤酒后,其体内每100mL血液中乙醇的含量(理论上)升高 mg, (填影响或不影响)其驾车或操作机器的能力。
Ⅳ.节能、减排、低碳、环保是当今世界的主旋律。
开发 等新能源(举一例),不仅可以部分解决化石能源紧缺问题,还可以减少对环境的污染。
煤燃烧时,可能产生SO2气体和氮的氧化物等有害气体排放,引起酸雨。
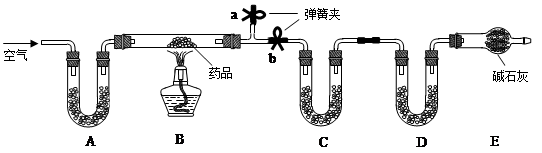
模拟酸雨形成的流程如下图所示。硫在单质气体A中燃烧发出蓝紫色火焰,生成刺激性气味的气体B;通常情况下C为最常见的无色液体,B、C、D是氧化物;E、F和X都是酸,G是既不溶于水又不溶于硝酸的白色沉淀。

试填空。
(1)E的化学式为: 。
(2)反应①的化学方程式为: 。
(3)反应④的化学方程式为: 。
(4)反应⑥的化学方程式为: 。
Ⅰ.食品、药物安全一直是人们关注的话题。
⑴2012年4月17日经央视新闻频道曝光的用工业明胶制成的医用“毒胶囊”震惊全国。据悉,其中混有的重金属铬对人体有害。这里的铬是指 (填“元素”或“单质”或“元素”)。
⑵我市盛产的海产品鱼虾中富含基本营养素(糖类、油脂、蛋白质、维生素)中的 。
Ⅱ.材料的应用与发展,大大方便了人们的生活。请用下列三种材料的对应字母填空。
A.有机合成材料 B.金属材料 C.天然有机高分子材料 D、无机非金属材料
⑴塑料制品属于 。
⑵蚕丝、羊毛、棉花属于 。
⑶可用于制造人造骨、航天飞机等的钛合金属于 。
Ⅲ.随着人们生活水平的提高,私家车拥有量越来越多,酒驾会对人和社会造成非常不良的后果。
啤酒、红酒和白酒中都含有乙醇(C2H5OH),饮酒后乙醇可进入人体血液中,科学实验表明,当乙醇在人体血液中的含量超过80mg /100mL血(每100mL血中含有80mg乙醇)时,便会影响人的驾车或操作机器的能力;已知饮用某啤酒1大杯(0.56L),会使血液中乙醇含量升高30mg/100mL血。回答下列问题:
(1)乙醇分子中碳、氢、氧原子个数比是 。写出乙醇燃烧的化学方程式 。
(2)李明饮用了3大杯上述啤酒后,其体内每100mL血液中乙醇的含量(理论上)升高 mg, (填影响或不影响)其驾车或操作机器的能力。
Ⅳ.节能、减排、低碳、环保是当今世界的主旋律。
开发 等新能源(举一例),不仅可以部分解决化石能源紧缺问题,还可以减少对环境的污染。
煤燃烧时,可能产生SO2气体和氮的氧化物等有害气体排放,引起酸雨。
模拟酸雨形成的流程如下图所示。硫在单质气体A中燃烧发出蓝紫色火焰,生成刺激性气味的气体B;通常情况下C为最常见的无色液体,B、C、D是氧化物;E、F和X都是酸,G是既不溶于水又不溶于硝酸的白色沉淀。

试填空。
(1)E的化学式为: 。
(2)反应①的化学方程式为: 。
(3)反应④的化学方程式为: 。
(4)反应⑥的化学方程式为: 。
Ⅰ.(1)元素;(2)蛋白质;
Ⅱ.(1)A;(2)C;(3)B;
Ⅲ.(1)2:6:1; C2H5OH + 3O2 2CO2 + 3H2O;(2)90;影响;
2CO2 + 3H2O;(2)90;影响;
Ⅳ.太阳能等;(1).E的化学式为H2SO3;(2)S + O2 SO2;(3)S03+H2O=H2SO4;
SO2;(3)S03+H2O=H2SO4;
(4)Na2SO4+BaCl2=BaSO4↓+2NaCl;
Ⅱ.(1)A;(2)C;(3)B;
Ⅲ.(1)2:6:1; C2H5OH + 3O2
 2CO2 + 3H2O;(2)90;影响;
2CO2 + 3H2O;(2)90;影响;Ⅳ.太阳能等;(1).E的化学式为H2SO3;(2)S + O2
 SO2;(3)S03+H2O=H2SO4;
SO2;(3)S03+H2O=H2SO4;(4)Na2SO4+BaCl2=BaSO4↓+2NaCl;
试题分析:Ⅰ.(1)“毒胶囊”中 混有的重金属铬对人体有害。是以无机盐的形式存在,故这里的铬是指元素;⑵海产品鱼虾中富含基本营养素蛋白质;Ⅱ.材料的应用与发展,大大方便了人们的生活。⑴塑料制品属于有机合成材料;⑵蚕丝、羊毛、棉花属于天然有机高分子材料;⑶可用于制造人造骨、航天飞机等的钛合金属于金属材料;Ⅲ. (1)乙醇分子中碳、氢、氧原子个数比是2:6:1。乙醇燃烧的化学方程式为:C2H5OH + 3O2
 2CO2 + 3H2O; (2)李明饮用了3大杯上述啤酒后,其体内每100mL血液中乙醇的含量(理论上)升高90mg,影响其驾车或操作机器的能力。Ⅳ.开发太阳能等可以部分解决化石能源紧缺问题,还可以减少对环境的污染;依据题中的叙述可以推断出 ;(1)E的化学式为:H2SO3;(2)反应①的化学方程式为:S + O2
2CO2 + 3H2O; (2)李明饮用了3大杯上述啤酒后,其体内每100mL血液中乙醇的含量(理论上)升高90mg,影响其驾车或操作机器的能力。Ⅳ.开发太阳能等可以部分解决化石能源紧缺问题,还可以减少对环境的污染;依据题中的叙述可以推断出 ;(1)E的化学式为:H2SO3;(2)反应①的化学方程式为:S + O2 SO2; (3)反应④的化学方程式为S03+H2O=H2SO4;(4)反应⑥的化学方程式为: Na2SO4+BaCl2=BaSO4↓+2NaCl;
SO2; (3)反应④的化学方程式为S03+H2O=H2SO4;(4)反应⑥的化学方程式为: Na2SO4+BaCl2=BaSO4↓+2NaCl;
练习册系列答案
相关题目