题目内容
小明从实验室取出一根铝丝,投入稀盐酸溶液中,开始没有出现气泡,一段时间后铝丝
表面才开始冒气泡,请你用两个化学方程式解释所观察到的实验现象,并判断其反应类型.
(1) ( 反应)
(2) ( 反应)
为此将铝丝投入稀盐酸前必须将铝丝做 处理.
表面才开始冒气泡,请你用两个化学方程式解释所观察到的实验现象,并判断其反应类型.
(1)
(2)
为此将铝丝投入稀盐酸前必须将铝丝做
考点:金属的化学性质,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:根据铝和空气中的氧气反应会生成致密的氧化铝薄膜,氧化铝、铝都会与盐酸反应等知识进行分析.
解答:解:(1)氧化铝和盐酸反应生成氯化铝和水,该反应满足复分解反应的条件,属于复分解反应,化学方程式为:Al2O3+6HCl=2AlCl3+3H2O;
(2)铝和盐酸反应生成氯化铝和氢气,该反应满足置换后反应的条件,属于置换后反应,化学方程式为:2Al+6HCl=2AlCl3+3H2↑,所以在将铝丝与盐酸反应之前,必须先将表面的氧化铝除去,先做砂纸打磨处理.
故答案为:(1)Al2O3+6HCl=2AlCl3+3H2O,复分解;
(2)2Al+6HCl=2AlCl3+3H2↑,置换;砂纸打磨.
(2)铝和盐酸反应生成氯化铝和氢气,该反应满足置换后反应的条件,属于置换后反应,化学方程式为:2Al+6HCl=2AlCl3+3H2↑,所以在将铝丝与盐酸反应之前,必须先将表面的氧化铝除去,先做砂纸打磨处理.
故答案为:(1)Al2O3+6HCl=2AlCl3+3H2O,复分解;
(2)2Al+6HCl=2AlCl3+3H2↑,置换;砂纸打磨.
点评:本题主要考查了铝的化学性质,以及金属活动性顺序的应用,难度不大,注意方程式的配平.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
下列各组溶液,不加其他试剂就能鉴别的是( )
| A、NaOH溶液、NaCl溶液、KCl溶液、FeCl3溶液 |
| B、Na2CO3溶液、稀硫酸、稀盐酸、NaNO3溶液 |
| C、稀盐酸、AgNO3溶液、稀硝酸、MgCl2溶液 |
| D、K2SO4溶液、Na2CO3溶液、BaCl2溶液、稀硝酸 |
 如图是a、b、c三种物质的溶解度曲线,请据图回答:
如图是a、b、c三种物质的溶解度曲线,请据图回答: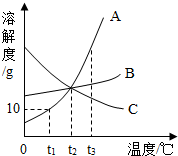 如图是A、B、C、三种物质的溶解度曲线,据图回答以下问题:
如图是A、B、C、三种物质的溶解度曲线,据图回答以下问题: