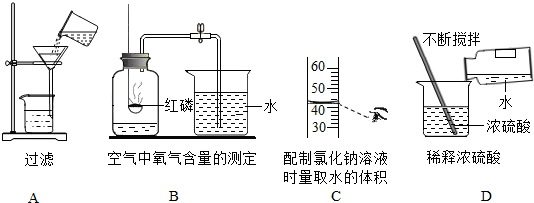
题目内容
30、下列是初中化学常见的物质,根据要求回答问题:
(1)A溶于水时放热,且水溶液中滴入紫色石蕊试液,溶液呈现红色,则A的化学式为
(2)红色固体B 遇A的稀溶液能形成黄色溶液,其变化的化学方程式是
(3)C、D、E、F分别属于酸、碱、盐、氧化物中的一种,且每两种物质相遇,其现象如图所示:(提示:碱、盐溶于水参与反应;“---”表示不反应或无现象,“↑”表示气体,“↓”表示沉淀)C与F反应的反应类型是
| C | |||
| --- | D | ||
| ↑ | --- | E | |
| --- | ↓ | ↓ | F |
浓H2SO4
.(2)红色固体B 遇A的稀溶液能形成黄色溶液,其变化的化学方程式是
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
.(3)C、D、E、F分别属于酸、碱、盐、氧化物中的一种,且每两种物质相遇,其现象如图所示:(提示:碱、盐溶于水参与反应;“---”表示不反应或无现象,“↑”表示气体,“↓”表示沉淀)C与F反应的反应类型是
复分解反应
;E与F反应的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
.当D、E相遇,且D过量时,会发生化合反应,其反应的化学方程式为Na2CO3+H2O+CO2=2NaHCO3
.分析:(1)根据水溶液遇到酸碱指示剂变色确定酸碱性,和常见物质溶于水后的温度变化进行分析;
(2)根据常见的红色固体和黄色溶液的特殊现象进行分析解答;
(3)根据E和C会生成气体,所以E、C就是碳酸盐和酸,D和E、F都会生成沉淀,所以E是碳酸钠,D就是二氧化碳,F是氢氧化钙,C就是盐酸,将推出的物质带入转换关系验证即可;
(2)根据常见的红色固体和黄色溶液的特殊现象进行分析解答;
(3)根据E和C会生成气体,所以E、C就是碳酸盐和酸,D和E、F都会生成沉淀,所以E是碳酸钠,D就是二氧化碳,F是氢氧化钙,C就是盐酸,将推出的物质带入转换关系验证即可;
解答:解:(1)A溶于水放出大量的热,说明A是浓硫酸、或氢氧化钠、氧化钙,水溶液中滴入紫色石蕊试液,溶液呈现红色,所以A的水溶液显酸性,故答案为:浓H2SO4;
(2)黄色的溶液中含有铁离子,和酸反应会生成铁离子的红色固体,只能是氧化铁,氧化铁和硫酸反应生成硫酸铁和水,故答案为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(3)E和C会生成气体,所以E、C就是碳酸盐和酸,D和E、F都会生成沉淀,所以E是碳酸钠,D就是二氧化碳,F是氢氧化钙,C就是盐酸,盐酸和氢氧化钙反应生成氯化钙和水,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和水,二氧化碳过量时,和碳酸钠会生成碳酸氢钠,各种物质都满足转换关系,
故答案为:复分解反应,Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,Na2CO3+H2O+CO2=2NaHCO3
(2)黄色的溶液中含有铁离子,和酸反应会生成铁离子的红色固体,只能是氧化铁,氧化铁和硫酸反应生成硫酸铁和水,故答案为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(3)E和C会生成气体,所以E、C就是碳酸盐和酸,D和E、F都会生成沉淀,所以E是碳酸钠,D就是二氧化碳,F是氢氧化钙,C就是盐酸,盐酸和氢氧化钙反应生成氯化钙和水,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和水,二氧化碳过量时,和碳酸钠会生成碳酸氢钠,各种物质都满足转换关系,
故答案为:复分解反应,Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,Na2CO3+H2O+CO2=2NaHCO3
点评:在解此类题时,首先分析出题中的特殊现象的物质,然后再根据推出的物质和题中的关系确定剩余的物质,最后验证.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目