题目内容
工业制硝酸时,发生反应:4NH3(氨气)+5O2
4NO+6H2O.下列对该反应的理解正确的是( )
| ||
| A.该反应属于置换反应 |
| B.参加反应的NH3与O2的质量比为4:5 |
| C.NH3中氮元素的化合价为-3 |
| D.反应中除NH3外其余三种物质均属于氧化物 |
A、置换反应的特征是反应物生成物均是由一种单质和一种化合物组成,而该反应的生成物是两种化合物,所以该反应不是置换反应;
B、依据方程式4NH3(氨气)+5O2
4NO+6H2O可知NH3与O2的质量比为4×17:5×32=17:40;
C、化合物中各元素的化合价代数和是零,由于NH3中氢的化合价是+1,所以氮元素的化合价为-3;
D、氧化物是有两种元素组成且其中一种元素为氧元素的化合物,故两种反应物都不是氧化物,而两种生成物均是氧化物;
故选C
B、依据方程式4NH3(氨气)+5O2
| ||
C、化合物中各元素的化合价代数和是零,由于NH3中氢的化合价是+1,所以氮元素的化合价为-3;
D、氧化物是有两种元素组成且其中一种元素为氧元素的化合物,故两种反应物都不是氧化物,而两种生成物均是氧化物;
故选C

练习册系列答案
相关题目
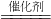 4NO+6H2O.下列对该反应的理解正确的是
4NO+6H2O.下列对该反应的理解正确的是 4NO+6H2O.下列对该反应的理解正确的是( )
4NO+6H2O.下列对该反应的理解正确的是( )