题目内容
根据如图所示实验装置回答问题: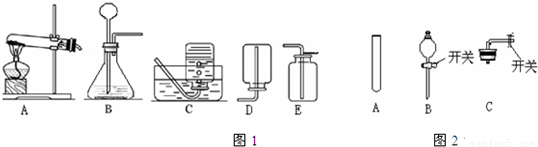
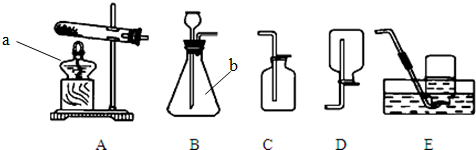
(1)小明同学选择A装置准备用高锰酸钾为原料制取一瓶纯净的氧气(不考虑水蒸气),他应选择的收集装置是______(填字母),写出该方法制取氧气的化学反应方程式______ K2MnO4+MnO2+O2↑
【答案】分析:制取装置包括加热和不需加热两种,如果用双氧水制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.当过氧化氢接触到二氧化锰后,反应便立即开始,不能人为控制其速度和生成氧气的量,如果把长颈漏斗换成分液漏斗,就可以控制反应的发生和停止;小华制取氧气的方法更好一些,因为反应在常温下进行节约能源;操作简便等;图1实验装置还可制取二氧化碳,实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.
解答:解:(1)如果用高锰酸钾制氧气就需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的气体比较纯净.故答案为:C; 2KMnO4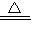 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
(2)如果用双氧水和二氧化锰制氧气就不需要加热,不需要加热的理由是:过氧化氢是液体、二氧化锰是固体,因此反应不要加热;氧气的密度比空气的密度大,因此能用向上排空气法收集;故答案为:B;过氧化氢是液体、二氧化锰是固体,反应不要加热;E
(3)当过氧化氢接触到二氧化锰后,反应便立即开始,不能人为控制其速度和生成氧气的量,如果把长颈漏斗换成分液漏斗,就可以控制反应的发生和停止;小华制取氧气的方法更好一些,因为反应在常温下进行节约能源;操作简便等;图1实验装置还可制取二氧化碳,实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.故答案为:B 长颈漏斗 ①小华; 反应在常温下进行节约能源、操作简便;②二氧化碳或CO2;大理石或石灰石,稀盐酸;CaCO3+2HCl=CaCl2+H2O+CO2↑
点评:本考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.
解答:解:(1)如果用高锰酸钾制氧气就需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的气体比较纯净.故答案为:C; 2KMnO4
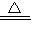 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑(2)如果用双氧水和二氧化锰制氧气就不需要加热,不需要加热的理由是:过氧化氢是液体、二氧化锰是固体,因此反应不要加热;氧气的密度比空气的密度大,因此能用向上排空气法收集;故答案为:B;过氧化氢是液体、二氧化锰是固体,反应不要加热;E
(3)当过氧化氢接触到二氧化锰后,反应便立即开始,不能人为控制其速度和生成氧气的量,如果把长颈漏斗换成分液漏斗,就可以控制反应的发生和停止;小华制取氧气的方法更好一些,因为反应在常温下进行节约能源;操作简便等;图1实验装置还可制取二氧化碳,实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.故答案为:B 长颈漏斗 ①小华; 反应在常温下进行节约能源、操作简便;②二氧化碳或CO2;大理石或石灰石,稀盐酸;CaCO3+2HCl=CaCl2+H2O+CO2↑
点评:本考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目