题目内容
小明的妈妈经常为小明蒸碱面馒头吃,有一次小明仔细查看了包装说明,发现此品牌纯碱中碳酸钠含量大于98%。他从家里带了一包样品来学校实验室检验其中的碳酸钠含量是否属实。现准确秤取6g试样放在烧杯中,并向其中滴加稀盐酸至恰好完全反应(忽略CO2溶于水)。共用去盐酸36.5g,此时烧杯内溶液总质量为40.3g(杂质溶于水,且不与稀盐酸反应)。试计算:
(1)生成CO2的质量是 。
(2)样品中碳酸钠的质量分数是多少?并判断样品中碳酸钠含量与标签是否相符。
(3)所用稀盐酸中溶质的质量分数是多少?
【答案】
(1)2.2g (2)88.3% 与标签不相符 (3)10%
【解析】
试题分析:(1)根据重量守恒定律可得:6g+36.5g-40.3g=2.2g
(2)设6g样品中含有碳酸钠的质量为x,
2HCl+Na2CO3═2NaCl+H2O+CO2↑
106 44
x 2.2g
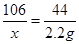
则:x=5.3g
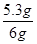 ×100%=88.3% ∵88.3%<98% ∴与标签不相符
×100%=88.3% ∵88.3%<98% ∴与标签不相符
(3)设所用盐酸的溶质质量分数为y,
2HCl+Na2CO3═2NaCl+H2O+CO2↑
73 44
36.5gXy 2.2g
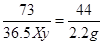
y=10%
考点:利用化学式计算。

练习册系列答案
相关题目
 了包装说明,发现此品
了包装说明,发现此品