题目内容
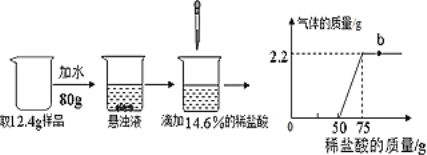
【题目】高纯氧化锌广泛应用于电子工业,某研究小组设计如下流程制备高纯氧化锌;

(1)反应①的化学方程式为______。
(2)反应②的基本反应类型是______;反应②后进行的分离操作名称是______。
(3)若得到的NH4Cl溶液有浑浊,原因可能是______(写出一种即可);农业上,氯化铵______(填“能”或“不能”)和尿素(CO(NH2)2)一起混合使用。
(4)反应③属于分解反应,除得到氧化锌外还生成两种常见气体,其化学式为______、______。
【答案】Zn+2HCl═ZnCl2+H2↑ 复分解反应 过滤 滤纸破损 能 CO2 CO
【解析】
(1)锌与稀盐酸反应生成氯化锌和氢气,化学方程式为:Zn+2HCl═ZnCl2+H2↑;
(2)由流程图和物质间的反应可知:②是氯化锌和草酸铵相互交换成分生成氯化铵和草酸锌沉淀,属于复分解反应,过滤可以将不溶性固体从溶液中分离出来,所以反应②后进行的分离操作名称是过滤;
(3)反应②后进行的分离操作名称是过滤,若得到的NH4Cl溶液有浑浊,原因可能是滤纸破损、液面高于滤纸边缘等,氯化铵和尿素都可以为农作物补充氮肥,二者不反应,农业上,氯化铵能和尿素CO(NH2)2一起混合使用;
(4)由质量守恒定律可知,化学反应前后元素的种类和质量不变,反应③属于分解反应,草酸锌分解除得到氧化锌外还生成CO2、CO。

练习册系列答案
相关题目