题目内容
【题目】合成氨工业中,常用碳酸钾溶液吸收产生的二氧化碳得到碳酸氢钾,反应的化学方程式为![]() 。向一定质量的碳酸钾溶液中通入二氧化碳,恰好完全反应,得到
。向一定质量的碳酸钾溶液中通入二氧化碳,恰好完全反应,得到![]() 溶质质量分数为
溶质质量分数为![]() 的碳酸氢钾溶液。试计算:原碳酸钾溶液中溶质的质量分数(结果精确到
的碳酸氢钾溶液。试计算:原碳酸钾溶液中溶质的质量分数(结果精确到![]() )_______。
)_______。
【答案】![]() 。
。
【解析】
根据溶质质量分数的计算公式计算出碳酸氢钾的质量,由碳酸氢钾的质量可求出碳酸钾和二氧化碳的质量,在根据质量守恒定律和溶质质量分数的计算公式计算即可。
解:碳酸氢钾的质量为:40g×12.5%=5g,设碳酸钾的质量为x,二氧化碳的质量为y,
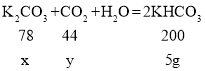
![]() x=1.95g,
x=1.95g,
![]() y=1.1g,
y=1.1g,
原碳酸钾溶液中溶质的质量分数是:![]() ×100%≈5.0%;
×100%≈5.0%;
答:原碳酸钾溶液中溶质的质量分数是5.0%。

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案【题目】实验室常用下列装置制取气体,请根据所学知识回答。
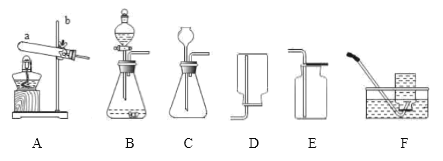
(1)写出图中仪器名称:a________________;b________________。
(2)实验室用A装置制取氧气。
I.反应的化学方程式为________________________,搭建A装置时,酒精灯应在固定仪器a之________(选填“前”或“后”)放置。
II.从反应后的剩余固体中回收得到二氧化锰的操作步骤顺序是________。(请填写编号)
①洗涤 ②过滤 ③烘干 ④溶解
(3)实验室在常温下用块状电石与水反应制取乙炔气体,该反应必须严格控制加水速度,以免引起发生装置炸裂。上图中最适合制取乙炔气体的发生装置是________(填装置编号)。
(4)选用F装置收集较纯净氧气的适宜时刻是________。也可选择E装置收集氧气,依据是________,证明氧气已集满的方法为________________。
(5)选用C装置,将一定量的双氧水和二氧化锰混合,充分反应,测得反应的总质量(m)与反应时间(t)的数据如下表所示:
反应时间t/s |
|
|
|
|
|
|
总质量m/g | 50 | 49.0 | 48.1 | 47.3 | 46.8 | 46.8 |
根据题目要求,回答下列问题:
I.双氧水和二氧化锰完全反应生成氧气的质量是________________;
II.分解的过氧化氢的物质的量是多少摩尔?(列式计算)________________________。
【题目】某国人大和政协会议使用了一种含碳酸钙的“石头纸”:为测定其中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品。分别在5只烧杯中进行了实验,实验数据见下表:(假设纸张其他成分既不溶于水,也不与水反应):
烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
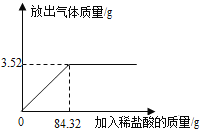
充分反应后生成 气体的质量/g | 0.88 | 1.76 | X | 3.52 | 3.52 |
(1)表中X的值为;______
(2)求样品中碳酸钙的质量分数;_____
(3)计算所用稀盐酸溶质的质量分数?_______