题目内容
【题目】向硫酸铜溶液中滴加氢氧化钠溶液至恰好完全反应。
(1)反应的化学方程式______________________________。
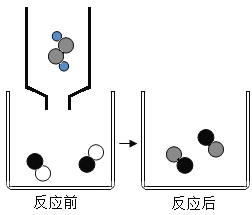
(2)如图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子。(填离子符号)
![]() ________
________ ![]() ________
________ ![]() ________
________
(3)下列物质中能与硫酸铜溶液发生反应,且基本反应类型相同的是___________(填选项)。
A.KOH B.BaCl2 C.Mg(OH)2 D.Fe
【答案】 CuSO4+2NaOH==Cu(OH)2↓+Na2SO4 Na+ Cu2+ SO42- AB
【解析】(1)根据反应物、生成物及复分解反应发生的条件解答;
(2)根据硫酸铜溶液中滴加氢氧化钠溶液至恰好完全反应分析;
(3)根据复分解反应发生的条件分析。
解:(1)向硫酸铜溶液中滴加氢氧化钠溶液至恰好完全反应。反应的化学方程式CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(2)根据反应实质CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,且由图可知,反应后溶液中的离子是Na+和SO42-,加入溶液中的离子是Na+和OH-,故![]() 表示 Na+,
表示 Na+,![]() 表示 Cu2+,
表示 Cu2+,![]() 表示 SO42-;
表示 SO42-;
(3)KOH与CuSO4反应生成Cu(OH)2沉淀;BaCl2 与CuSO4反应生成Ba SO4沉淀;Mg(OH)2和CuSO4不反应;Fe与CuSO4发生置换反应生成Cu和FeSO4。故
能与硫酸铜溶液发生反应,且基本反应类型相同的是KOH与BaCl2。故选AB。

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目