题目内容
【题目】深圳是海滨城市,海水资源丰富.镁被称为“国防金属”广泛地应用于火箭、飞机、轮船等制造业.工业上可从海水中提取镁,其物质的转化关系如图所示.(其中部分生成物已省略)根据以下转化关系,回答下列问题: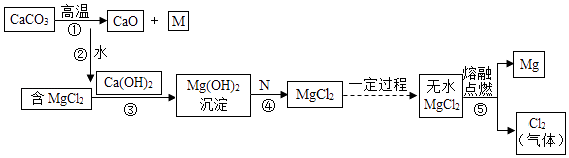
(1)M是一种常用于灭火的气体,M的化学式是 , 若在M的饱和溶液中滴入几滴紫色石蕊溶液,则溶液变色;
(2)反应过程中会(填“吸收”或“放出”)热量;
(3)反应属于反应(填基本反应类型);
(4)N是(只有一个正确选项,选填字母);
A.硫酸
B.盐酸
C.氢氧化钠溶液
D.氯化钠溶液
(5)写出反应④的化学方程式:;
(6)写出反应⑤的化学方程式: .
【答案】
(1)CO2;红
(2)吸收
(3)化合
(4)B
(5)Mg(OH)2+2HCl=MgCl2+2H2O
(6)MgCl2![]() Mg+Cl2↑
Mg+Cl2↑
【解析】解:(1)碳酸钙高温煅烧生成氧化钙和二氧化碳气体,则M是二氧化碳,二氧化碳与水反应生成碳酸,碳酸能使紫色的石蕊试液变红色;故填:CO2;红;(2)反应①是在高温煅烧的条件下进行的,所以该反应属于吸热反应,需要吸收热量;故填:吸收;(3)反应②是氧化钙与水反应生成氢氧化钙,该反应符合“多变一”的特征,属于化合反应;故填:化合;(4)该反应是由氢氧化镁这种难溶性的碱与N反应生成氯化镁这种盐,所以N是盐酸;故填:B;(5)反应④氢氧化镁与稀盐酸发生中和反应生成氯化镁和水;故填:Mg(OH)2+2HCl=MgCl2+2H2O;(6)反应⑤是氯化镁在通电的条件下生成镁和氯气;故填:MgCl2![]() Mg+Cl2↑.
Mg+Cl2↑.
【考点精析】解答此题的关键在于理解书写化学方程式、文字表达式、电离方程式的相关知识,掌握注意:a、配平 b、条件 c、箭号.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用15g石灰石样品,把50g稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如下:
实验次数 | 1 | 2 | 3 | 4 | 5 |
稀盐酸的累计加入量 | 10g | 20g | 30g | 40g | 50g |
剩余固体的质量 | 12g | 9g | 6g | 5g | 5g |
请计算:
(1)石灰石中碳酸钙的质量分数为多少?
(2)最终生成二氧化碳的质量是多少?