题目内容
(2012?仙桃)某学习小组做镁带在空气中燃烧实验时,发现生成物中有黑色固体.针对这一现象,他们开展了如下探究活动.请仔细阅读并完成下列探究报告.
【探究目的】探究镁在空气中燃烧产生的黑色固体是镁与空气中什么物质反应产生的.
【分析猜想】分析空气中各种成分,寻找猜想依据.
空气成分之一:
空气成分之二:氧气,与镁反应生成的氧化镁是
空气成分之三:水蒸气,打磨光亮的镁带放入沸水中,表面会附有白色固体并产生大量气泡;再向沸水中滴入无色酚酞试液,呈现红色.则镁在沸水中反应的化学方程式为:
空气成分之四:氮气、二氧化碳.猜想:可能是镁与N2或CO2反应生成黑色固体.
【实验一】镁带与氮气的反应
(一)获取氮气
(1)把空气液化,然后蒸发,先蒸发出来的气体就是氮气.这种方法属于
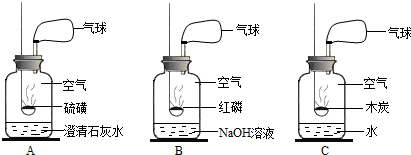
(2)以下是获取氮气的方法及装置,其中得到氮气较纯的是
(二)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛N2的集气瓶中,瓶内壁附着一层淡黄色的固体.
(三)实验结论:镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁.该反应
的化学方程式是
【实验二】将燃着的镁带伸入盛CO2的集气瓶中,镁带剧烈燃烧,瓶内出现白色固体和黑色固体.CO2与镁发生了置换反应,生成的黑色固体物质是
【探究结论】镁在空气中燃烧产生的黑色固体是镁与空气中CO2反应产生的.
【探究目的】探究镁在空气中燃烧产生的黑色固体是镁与空气中什么物质反应产生的.
【分析猜想】分析空气中各种成分,寻找猜想依据.
空气成分之一:
氮气
氮气
,化学性质稳定,一般不与其它物质反应.空气成分之二:氧气,与镁反应生成的氧化镁是
白
白
色固体.空气成分之三:水蒸气,打磨光亮的镁带放入沸水中,表面会附有白色固体并产生大量气泡;再向沸水中滴入无色酚酞试液,呈现红色.则镁在沸水中反应的化学方程式为:
Mg+2H2O=Mg(OH)2↓+H2↑
Mg+2H2O=Mg(OH)2↓+H2↑
. 如果将镁带放到水蒸气中,也会发生上述反应,但产生的不是黑色固体.空气成分之四:氮气、二氧化碳.猜想:可能是镁与N2或CO2反应生成黑色固体.
【实验一】镁带与氮气的反应
(一)获取氮气
(1)把空气液化,然后蒸发,先蒸发出来的气体就是氮气.这种方法属于
物理
物理
(选填“物理”或“化学”)方法.但在实验室里空气不易被液化.(2)以下是获取氮气的方法及装置,其中得到氮气较纯的是
B
B
.(填字母)
(二)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛N2的集气瓶中,瓶内壁附着一层淡黄色的固体.
(三)实验结论:镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁.该反应
的化学方程式是
3Mg+N2
Mg3N2
| ||
3Mg+N2
Mg3N2
.
| ||
【实验二】将燃着的镁带伸入盛CO2的集气瓶中,镁带剧烈燃烧,瓶内出现白色固体和黑色固体.CO2与镁发生了置换反应,生成的黑色固体物质是
碳
碳
.【探究结论】镁在空气中燃烧产生的黑色固体是镁与空气中CO2反应产生的.
分析:【分析猜想】根据空气的成分及各成分的化学性质、常见化学物质的物理性质、化学方程式的书写方法进行分析解答.
【实验一】(一)(1)根据题意,把空气液化,然后蒸发,先蒸发出来的气体就是氮气,根据是否有新物质生成,确定利用的是物理方法还是化学方法.
(2)将空气中氧气除去得到较纯净的氮气,所选除氧剂要具备以下特征:(1)本身能够在空气中燃烧;(2)本身的状态为非气体;(3)生成的物质为非气态.
(三)根据题意,写出反应的化学方程式即可.
【实验二】CO2与镁发生了置换反应,根据质量守恒定律,可以确定生成的黑色固体的成分.
【实验一】(一)(1)根据题意,把空气液化,然后蒸发,先蒸发出来的气体就是氮气,根据是否有新物质生成,确定利用的是物理方法还是化学方法.
(2)将空气中氧气除去得到较纯净的氮气,所选除氧剂要具备以下特征:(1)本身能够在空气中燃烧;(2)本身的状态为非气体;(3)生成的物质为非气态.
(三)根据题意,写出反应的化学方程式即可.
【实验二】CO2与镁发生了置换反应,根据质量守恒定律,可以确定生成的黑色固体的成分.
解答:解:【分析猜想】空气成分之一:空气中的氮气化学性质不活泼,一般不与其它物质反应.
空气成分之二:氧化镁是白色的固体.
空气成分之三:根据题意,镁与沸水反应,表面会附有白色固体并产生大量气泡;再向沸水中滴入无色酚酞试液,呈现红色,说明有碱性物质生成;根据质量守恒定律,生成的气体为氢气,反应的化学方程式为:Mg+2H2O=Mg(OH)2↓+H2↑.
【实验一】(一)获取氮气:(1)把空气液化,然后蒸发,先蒸发出来的气体就是氮气,分离过程中没有新物质生成,属于物理方法.
(2)硫磺在空气中能够燃烧生成二氧化硫气体,虽除去氧气,而增加了新的气体二氧化硫,尽管石灰水能吸收二氧化硫,但由于氢氧化钙的溶解度较小,石灰水中溶解的氢氧化钙较少,不能全部吸收二氧化硫,不能得到较纯净的氮气.
红磷本身是固体,在空气中燃烧,且生成物五氧化二磷是固体,可以用于除去空气中的氧气;且氢氧化钠溶液能吸收空气中的二氧化碳,能得到较纯的氮气.
木炭在空气中燃烧生成二氧化碳气体或者一氧化碳气体甚至是两者的混合气体,虽除去氧气,而增加了新的气体,不能得到较纯净的氮气.
(三)镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁,反应的化学方程式为:3Mg+N2
Mg3N2.
【实验二】将燃着的镁带伸入盛CO2的集气瓶中,镁带剧烈燃烧,瓶内出现白色固体和黑色固体.CO2与镁发生了置换反应,生成物为氧化镁和碳,黑色固体物质是碳.
答案为:氮气;白;Mg+2H2O=Mg(OH)2↓+H2↑;物理;B;3Mg+N2
Mg3N2;碳.
空气成分之二:氧化镁是白色的固体.
空气成分之三:根据题意,镁与沸水反应,表面会附有白色固体并产生大量气泡;再向沸水中滴入无色酚酞试液,呈现红色,说明有碱性物质生成;根据质量守恒定律,生成的气体为氢气,反应的化学方程式为:Mg+2H2O=Mg(OH)2↓+H2↑.
【实验一】(一)获取氮气:(1)把空气液化,然后蒸发,先蒸发出来的气体就是氮气,分离过程中没有新物质生成,属于物理方法.
(2)硫磺在空气中能够燃烧生成二氧化硫气体,虽除去氧气,而增加了新的气体二氧化硫,尽管石灰水能吸收二氧化硫,但由于氢氧化钙的溶解度较小,石灰水中溶解的氢氧化钙较少,不能全部吸收二氧化硫,不能得到较纯净的氮气.
红磷本身是固体,在空气中燃烧,且生成物五氧化二磷是固体,可以用于除去空气中的氧气;且氢氧化钠溶液能吸收空气中的二氧化碳,能得到较纯的氮气.
木炭在空气中燃烧生成二氧化碳气体或者一氧化碳气体甚至是两者的混合气体,虽除去氧气,而增加了新的气体,不能得到较纯净的氮气.
(三)镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁,反应的化学方程式为:3Mg+N2
| ||
【实验二】将燃着的镁带伸入盛CO2的集气瓶中,镁带剧烈燃烧,瓶内出现白色固体和黑色固体.CO2与镁发生了置换反应,生成物为氧化镁和碳,黑色固体物质是碳.
答案为:氮气;白;Mg+2H2O=Mg(OH)2↓+H2↑;物理;B;3Mg+N2
| ||
点评:本题难度较大,考查同学们新信息获取、处理及灵活运用所学化学知识进行分析问题、解决问题的能力.

练习册系列答案
相关题目



