题目内容
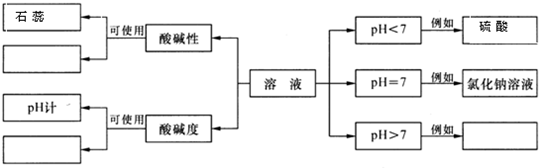
(1)概念图对一些知识点进行整理,十分有用.请根据下图中的示例,在空的“□”中填写相应物质的名称.(注:pH计是一种测pH的仪器)
(2)向盛有10mL稀盐酸(其中滴有少量紫色石蕊溶液)的烧杯中加入氢氧化钠溶液,用pH计测定溶液的pH,所得数据如下.请分析并回答下列问题:
| 加入NaOH溶液的体积/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
②当烧杯中溶液的pH=1.4时,溶液中的溶质有(化学式) 、 .
(3)某同学想探究酸碱中和反应是放热反应.进行下列实验操作:取溶质质量分数为20%的稀硫酸30mL,用温度计测出其温度为13℃.然后向其中加入5.6gNaOH固体,恰好完全反应.再用温度计测出温度为22℃.由此,该同学得出NaOH与稀硫酸发生的中和反应是放热反应的结论.该同学所得的结论是否科学?请说明理由 .
【答案】分析:(1)根据物质的分类:测酸碱性用的是酸碱指示剂,测酸碱度用的是PH试纸和PH计,再结合常见的酸碱盐来填空;(2)①根据紫色石蕊溶液遇到酸碱的变色情况考虑;②根据pH=1.4看谁过量;(3)根据氢氧化钠溶于水放热考虑.
解答:解:(1)测酸碱性用的是酸碱指示剂,常见的酸碱指示剂有:无色酚酞、紫色石蕊试液;测酸碱度用的是PH试纸和PH计;PH>7的是显碱性的物质例如氢氧化钠等;
(2)①当加入氢氧化钠溶液的体积为13mL时,PH>7了显碱性,所以紫色石蕊试液变蓝;
②当烧杯中溶液的pH=1.4时,说明显酸性,即还含有没反应的氯化氢,还有氢氧化钠与盐酸反应生成的氯化钠;
(3)由于氢氧化钠固体溶于水放出热量,所以温度的升高到底是中和反应放出的热量还是氢氧化钠固体溶于水放出的热量.
故答案为:(1)酚酞(或酚酞溶液) pH试纸 氢氧化钠溶液(或其他碱性溶液)
(2)①蓝 ②HCl NaCl (3)不科学,因为NaOH固体溶解也会放出大量的热
点评:解答本题的关键是要对所学的知识进行分类,知道紫色石蕊溶液遇到酸碱的变色情况,知道反应后溶质判断时要结合过量物质.
解答:解:(1)测酸碱性用的是酸碱指示剂,常见的酸碱指示剂有:无色酚酞、紫色石蕊试液;测酸碱度用的是PH试纸和PH计;PH>7的是显碱性的物质例如氢氧化钠等;
(2)①当加入氢氧化钠溶液的体积为13mL时,PH>7了显碱性,所以紫色石蕊试液变蓝;
②当烧杯中溶液的pH=1.4时,说明显酸性,即还含有没反应的氯化氢,还有氢氧化钠与盐酸反应生成的氯化钠;
(3)由于氢氧化钠固体溶于水放出热量,所以温度的升高到底是中和反应放出的热量还是氢氧化钠固体溶于水放出的热量.
故答案为:(1)酚酞(或酚酞溶液) pH试纸 氢氧化钠溶液(或其他碱性溶液)
(2)①蓝 ②HCl NaCl (3)不科学,因为NaOH固体溶解也会放出大量的热
点评:解答本题的关键是要对所学的知识进行分类,知道紫色石蕊溶液遇到酸碱的变色情况,知道反应后溶质判断时要结合过量物质.

练习册系列答案
相关题目
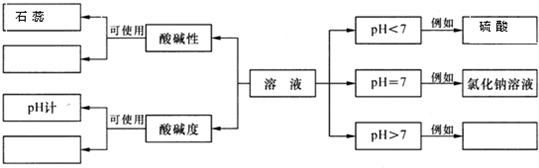
(1)概念图对一些知识点进行整理,十分有用.请根据下图中的示例,在空的“□”中填写相应物质的名称.(注:pH计是一种测pH的仪器)
(2)向盛有10mL稀盐酸(其中滴有少量紫色石蕊溶液)的烧杯中加入氢氧化钠溶液,用pH计测定溶液的pH,所得数据如下.请分析并回答下列问题:
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
②当烧杯中溶液的pH=1.4时,溶液中的溶质有(化学式)______、______.
(3)某同学想探究酸碱中和反应是放热反应.进行下列实验操作:取溶质质量分数为20%的稀硫酸30mL,用温度计测出其温度为13℃.然后向其中加入5.6gNaOH固体,恰好完全反应.再用温度计测出温度为22℃.由此,该同学得出NaOH与稀硫酸发生的中和反应是放热反应的结论.该同学所得的结论是否科学?请说明理由______.