题目内容
维生素C又名抗坏血酸,易溶于水,易被氧化,遇热易被破坏,人体缺乏维生素C可能引发多种疾病,它的化学式是C6H8O6,计算:
(1)维生素C中含有 种元素,其相对分子质量为 ;
(2)维生素C中氢元素的质量分数为 (结果保留一位小数)。
(3)现要配制溶质质量分数为2%的维生素C溶液500kg,需要25%的维生素C溶液的质量是 kg。
(1)维生素C中含有 种元素,其相对分子质量为 ;
(2)维生素C中氢元素的质量分数为 (结果保留一位小数)。
(3)现要配制溶质质量分数为2%的维生素C溶液500kg,需要25%的维生素C溶液的质量是 kg。
(1)3;176;(2)4.5%;(3)40
试题分析:(1)根据维生素C化学式的含义、相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答。
(2)根据化合物中元素的质量分数=
 ×100%,进行分析解答。
×100%,进行分析解答。(3)利用溶质质量=溶液质量×溶质的质量分数、溶液稀释前后溶质的质量不变进行分析解答。
解:(1)维生素C是由碳、氢、氧三种元素组成的;其相对分子质量为12×6+1×8+16×6=176。
(2)维生素C中氢元素的质量分数为
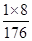 ×100%≈4.5%。
×100%≈4.5%。(3)设需要25%的维生素C溶液的质量是x,由题意,则500kg×2%=x×25%,x=40kg。
专题:化学式的计算;溶液的组成及溶质质量分数的计算

练习册系列答案
相关题目

 的化学式量为___________;
的化学式量为___________;