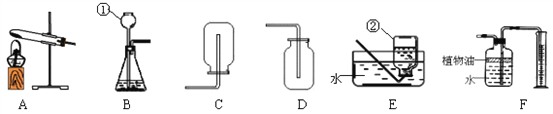
题目内容
【题目】如图为某加钙食盐包装袋袋上的标签.小明通过下列方法检查该食盐中的钙元素的含量:往装有稀硝酸的小烧杯(总质量为200.00g)加入30.00g该盐样品,充分反应后,无固体剩余.反应后烧杯和溶液的总质量为229.67g.
(已知:CaCO3+2HNO3=Ca(NO3)2+H2O+CO2↑)

(1)反应过程中产生_____g CO2
(2)30.00g该食盐中含碳酸钙的质量是多少______?
(3)此加钙食盐钙含量是否符合标签要求?_____.
【答案】0.33g 0.75g 1.3%>1.0%>0.3%
【解析】
(1)据质量守恒定律可知,反应前后物质的总质量不变,反应过程中产生二氧化碳的质量为:200.00g+30.00g-229.67g= 0.33g;
(2)设30.00g该食盐中含碳酸钙的质量是x
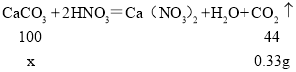
![]() x=0.75g
x=0.75g
钙元素的质量:![]() =0.3g
=0.3g
此加钙食盐钙含量是:0.3g÷30g×100%=1%
1.3%>1.0%>0.3%,符合要求。

【题目】在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种。同学们为了确定该粉末的成分,进行如下探究。请你参与他们的探究并回答问题。
(查阅资料)铜和氧化铁是红色固体,铁粉是黑色固体。
(1)(提出问题)
假设1:红色粉末是铜粉;假设2:红色粉末是氧化铁粉;假设3:红色粉末是___。
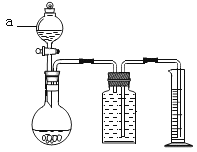
(设计实验方案)同学们对实验作了如下设想和取少量红色粉末放入硬质玻璃管中,通入一氧化碳片刻后加热至充分反应(实验装置如图所示)。
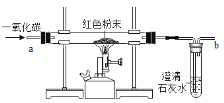
请你完成下表:
实验中可能出现的现象 | 结论 |
A红色粉末_______,石灰水_____ | 假设1成立 |
B红色粉末_________,石灰水变浑浊 | 假设2成立 |
C红色粉末部分变黑。石灰水________ | 假设3成立 |
(进行实验)通过实验及分析,确认假设3成立。
(2)(反思与评价)
①实验过程中,硬质玻璃管内发生反应的化学方程式是____。
②实验时通入一氧化碳片刻后再加热的原因是_____。
③从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是___。
(3)(拓展)为了把实验结束后的铜粉和铁粉分离开来,你认为可选用____(填序号)
A 过滤 B 用磁铁吸引 C 在空气中灼烧