题目内容
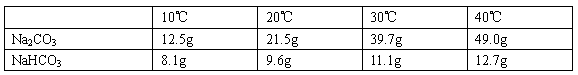
以下是Na2CO3和NaHCO3的溶解度表及溶解度曲线.根据图表回答下列问题:| 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
(2)欲使接近饱和的Na2CO3溶液变饱和,可采用的方法是______.
(3)已知Na2CO3转化为NaHCO3的反应为:Na2CO3+CO2+H2O=2NaHCO3,根据以上信息,向20℃饱和Na2CO3溶液中能入足量CO2气体,可观察到的现象是______(只写一种).

【答案】分析:由溶解度曲线图可知,不同物质在同一温度时的溶解度大小情况,也可知,同一物质在不同温度时的溶解度变化情况.
解答:解:(1)由图表可知,碳酸钠的溶解度在同一温度时比碳酸氢钠的溶解度大,所以a表示碳酸钠的溶解度.
(2)由溶解度曲线图可知,碳酸钠的溶解度随温度的升高而升高,所以欲使接近饱和的Na2CO3溶液变饱和,可采用降低温度的方法.
(3)由图表可知,碳酸氢钠的溶解度比碳酸钠的溶解度小,所以当通入二氧化碳时,二氧化碳与碳酸钠生成碳酸氢钠,碳酸氢钠的溶解度小,所以有大量的晶体析出.
故答案为:
(1)a.
(2)降温.
(3)有晶体析出.
点评:碳酸氢钠比碳酸钠的溶解度小,所以我们在海水制碱时,在饱和氨盐水中通入二氧化碳时,会有晶体析出.
解答:解:(1)由图表可知,碳酸钠的溶解度在同一温度时比碳酸氢钠的溶解度大,所以a表示碳酸钠的溶解度.
(2)由溶解度曲线图可知,碳酸钠的溶解度随温度的升高而升高,所以欲使接近饱和的Na2CO3溶液变饱和,可采用降低温度的方法.
(3)由图表可知,碳酸氢钠的溶解度比碳酸钠的溶解度小,所以当通入二氧化碳时,二氧化碳与碳酸钠生成碳酸氢钠,碳酸氢钠的溶解度小,所以有大量的晶体析出.
故答案为:
(1)a.
(2)降温.
(3)有晶体析出.
点评:碳酸氢钠比碳酸钠的溶解度小,所以我们在海水制碱时,在饱和氨盐水中通入二氧化碳时,会有晶体析出.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
以下是Na2CO3和NaHCO3的溶解度表及溶解度曲线.根据图表回答下列问题:
| 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
 (1)Na2CO3的溶解度曲线应为________(填“a”或“b”).
(1)Na2CO3的溶解度曲线应为________(填“a”或“b”).(2)欲使接近饱和的Na2CO3溶液变饱和,可采用的方法是________.
(3)已知Na2CO3转化为NaHCO3的反应为:Na2CO3+CO2+H2O=2NaHCO3,根据以上信息,向20℃饱和Na2CO3溶液中能入足量CO2气体,可观察到的现象是________(只写一种).
以下是Na2CO3和NaHCO3的溶解度表及溶解度曲线.根据图表回答下列问题:
(1)Na2CO3的溶解度曲线应为______(填“a”或“b”).
(2)欲使接近饱和的Na2CO3溶液变饱和,可采用的方法是______.
(3)已知Na2CO3转化为NaHCO3的反应为:Na2CO3+CO2+H2O=2NaHCO3,根据以上信息,向20℃饱和Na2CO3溶液中能入足量CO2气体,可观察到的现象是______(只写一种).

| 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
(2)欲使接近饱和的Na2CO3溶液变饱和,可采用的方法是______.
(3)已知Na2CO3转化为NaHCO3的反应为:Na2CO3+CO2+H2O=2NaHCO3,根据以上信息,向20℃饱和Na2CO3溶液中能入足量CO2气体,可观察到的现象是______(只写一种).