题目内容
【题目】【2016年山西省】炎热的夏天,在家中可以自制汽水来消暑消热。
【制备材料】1.5g小苏打、1.5g柠檬酸、蔗糖、果汁、凉开水、500ml饮料瓶
【制备流程】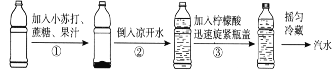 [
[
(1)下列是制汽水的操作或现象的相关问题,请选择I或II进行解答 。
I.步骤②中为什么要用凉开水制汽水?
II.步骤③旋紧瓶盖后,为什么汽水中的气泡会由多变少直至不再冒出?
(2)制汽水时,小苏打中的HCO3-与柠檬溶液中的H+反应生成的气体是 _____ 。为证明柠檬酸溶液中有H+,可以选择下列物质中的 进行验证(填字母,符合题意的选项都选)。
A.镁带 B.铜片 C.食盐 D.鸡蛋壳 e.石蕊溶液
【答案】(1)选择Ⅰ:凉开水温度较低,CO2的溶解度随温度的降低而增大 选择Ⅱ:旋紧瓶盖后,瓶内的压强增大,所以增大了CO2的溶解度
(2)CO2; ade
【解析】(1)在制取汽水时,先向瓶中加入小苏打、蔗糖、果汁,然后加入凉开水,再加入柠檬酸, 迅速盖上瓶盖,摇匀、冷藏,就得到汽水。选择Ⅰ:凉开水温度较低,CO2的溶解度随温度的降低而增大,当打开瓶塞时,CO2从瓶中溢出,水的温度降低,就可以起到降温、解渴的作用。II.步骤③旋紧瓶盖后,瓶内的压强增大,所以增大了二氧化碳的溶解度,所以会看到汽水中的气泡会由多变少直至不再冒出。(2)制汽水时,小苏打中的HCO3-与柠檬溶液中的H+反应生成的气体是CO2,要证明柠檬酸溶液中有H+,可以A.镁带可以与酸发生反应产生氢气,有大量的气泡溢出,可以证明,正确;B.铜活动性比H+小,不能与酸发生置换反应产生氢气,错误;C.食盐与酸不能发生反应,因此不能证明H+的存在,错误;D.鸡蛋壳主要成分是CaCO3,可以与H+发生反应产生CO2气体,有气泡溢出,古可以证明柠檬酸溶液中有H+,正确;e.石蕊溶液遇酸会变为红色,可以证明,正确。

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案