题目内容
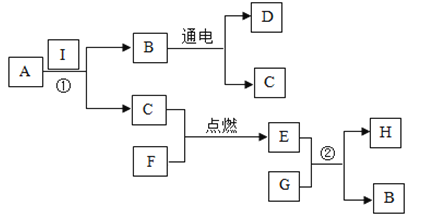
【题目】利用海水(含氯化钠)处理含二氧化硫的废气,该方法的流程如图:
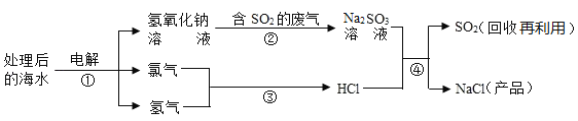
下列说法正确的是
A.海水中含有氯化钠,上述从海水得到“NaCl(产品)”的过程属于物理变化
B.①中参加反应的物质有氯化钠和水
C.反应②属于复分解反应
D.此反应流程有助于减少大气污染,保护环境
【答案】BD
【解析】
A、根据上述流程可知,从海水最终得到“NaCl(产品)”是反应生成的氯化钠,该变化属于化学变化,错误;
B、①中的反应物是氯化钠和水反应生成氢氧化钠和氢气和氯气,反应的化学方程式为:2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑,正确;
2NaOH+H2↑+Cl2↑,正确;
C、复分解反应是指两种化合物相互交换成分生成另外两种化合物的反应,反应②是氢氧化钠与二氧化硫反应生成亚硫酸钠和水,不属于复分解反应,错误;
D、由题意可知,“利用海水(含氯化钠)处理含二氧化硫的废气”,最后回收利用二氧化硫,此反应流程有助于减少大气污染,保护环境,正确;
故选BD。

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案【题目】某化学小组经查阅资料发现:镁除了能与氧气、盐酸、硫酸铜溶液反应,还能与饱和碳酸氢钠溶液反应。该组同学对镁的这种化学性质产生了兴趣,设计了如下实验方案进行探究:
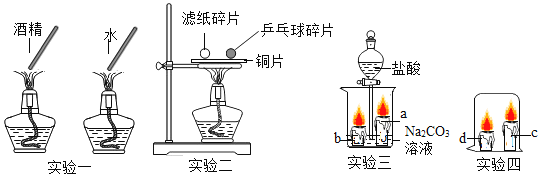
活动一:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量的气泡和白色不溶物。
(1)收集并点燃产生的气体,火焰呈淡蓝色,火焰上方罩涂有澄清石灰水的小烧杯,无现象。则该气体为_____。
(2)同学们对白色不溶物做出如下猜测:
(猜想假设)①白色不溶物可能是Mg(OH)2;
②白色不溶物可能是MgCO3;
③白色不溶物可能是_____。活动二:设计定量实验确定白色不溶物成分。
(查阅资料)①碱石灰主要成分是NaOH和CaO的混合物。
②MgCO3、Mg(OH)2加热易分解,分别生成两种氧化物。
请写出MgCO3加热分解的化学方程式:_____。
(进行实验)
操作 | 现象 | 结论 |
①取反应结束洗净后的白色不溶物,加入足量的_____。 | 观察到_____ | 白色固体一定含有MgCO3 |
②称取一定量白色不溶物,充分加热至不再产生气体,将产生的气体先通入碱石灰,再通入浓硫酸,分别称量装置反应前后的质量 | _____ | 白色固体只含有MgCO3 |
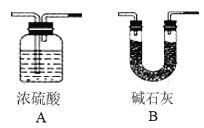
(反思评价)同学们通过计算发现上述结论不正确,原因_____,他们通过讨论对上述实验又进行了改进,则该装置的正确连接顺序(装置可重复使用且每步反应均能完全进行):加热不溶物产生的气体→_____(填装置序号)
【题目】氢氧化钡与氢氧化钙同属于碱类物质,其化学性质相似吗?某兴趣小组的同学对此进行探究。
Ⅰ.定性探究
序号 | 操作 | 现象 | 结论 |
实验一 | 向氢氧化钡溶液中滴入_____试剂 | 溶液变红 | 氢氧化钡溶液呈碱性 |
实验二 | 向实验一的溶液中通入适量的二氧化碳 | 产生_____, 红色消失 | 氢氧化钡溶液能与 二氧化碳反应 |
实验三 | 另取氢氧化钡溶液,滴入一定量 的碳酸钠溶液 | 产生白色沉淀 | 氢氧化钡溶液能与 碳酸钠溶液反应 |
(1)写出实验三中发生反应的化学方程式_____;
同学们将上述三个实验中反应后的废液都倒入一个烧杯中,过滤后,得到白色沉淀和红色滤液,他们决定对沉淀和滤液进行探究。
探究一:(提出问题)沉淀能否与酸发生反应?
(实验探究)向沉淀中加入足量的稀硫酸,观察到有气泡产生,最终沉淀_____(填“消失”或“不消失”)。
探究二:(提出问题)滤液中除指示剂外,还有哪些溶质?
(作出猜想)①氢氧化钠, ②氢氧化钠、碳酸钠, ③_____。
(实验探究)
序号 | 操作 | 现象 | 结论 |
实验四 | 取滤液样品于试管中, 加入几滴稀盐酸 | 没有明显现象 | 猜想②不成立 |
实验五 | 取滤液样品于试管中, 加入几滴碳酸钠溶液 | 产生沉淀 | 猜想_____成立 |
(2)有同学提出:实验四的操作存在问题,导致结论不准确,请你改正:_____。
(3)小组同学讨论后发现,只用一种溶液做一次实验,就可以验证猜想,该溶液是_____。
Ⅱ.定量探究
向100g氢氧化钡溶液中滴加溶质质量分数为10%的硫酸铜溶液,溶液的导电能力随着硫酸铜溶液的加入发生如图的变化关系。
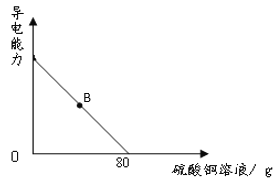
(1)溶液处于B点时,其中含有的是_____、_____、_____(填微粒符号)。
(2)计算氢氧化钡溶液的溶质质量分数_____。