题目内容
某固体混合物由Mg和MgO组成,取该混合物6.4g与一定量稀硫酸恰好完全反应(反应后溶液中无晶体析出),所得溶液中溶质的质量为24g,则原混合物中氧元素的质量为
| A.4.8g | B.1.6g | C.3.2g | D.2.56g |
B
解析试题分析:镁与稀硫酸反应生成硫酸镁和氢气;氧化镁与与稀硫酸反应生成硫酸镁和水。反应为恰好完全反应,则所得溶液中的溶质只有硫酸镁。根据溶质的质量为24g可知,含镁元素的质量为:24g×(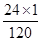 ×100%)=4.8g。所以原混合物中镁元素的质量也为4.8g。则原混合物中氧元素的质量为:6.4g —4.8g=1.6g。所以应选B项。
×100%)=4.8g。所以原混合物中镁元素的质量也为4.8g。则原混合物中氧元素的质量为:6.4g —4.8g=1.6g。所以应选B项。
考点:根据化学式的计算

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
煅烧石灰石(石灰石中的杂质不含钙、碳元素,且不参与反应)可制得氧化钙。测得煅烧后剩余固体中钙元素与碳元素的物质的量之比为2:1,则已分解的碳酸钙与原碳酸钙的质量比是
| A.3:5 | B.1:2 | C.2:5 | D.3:10 |
已知某种NH4NO3样品中混有不含氮元素的杂质,测得该NH4NO3样品中含氮的质量分数为24.5%,则样品中NH4NO3的质量分数为
| A.24.5% | B.49% | C.70% | D.80% |
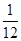 是1.67
是1.67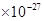 kg,又知氧的相对原子质量是16,一个氢原子的质量约为1.674
kg,又知氧的相对原子质量是16,一个氢原子的质量约为1.674