题目内容
【题目】将5%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.边回答: 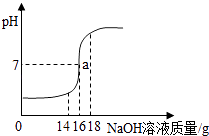
(1)a点溶液中大量存在的离子有;
(2)当恰好完全反应时,消耗NaOH溶液的质量为;
(3)计算稀盐酸中溶质的质量分数.
【答案】
(1)Na+、Cl﹣
(2)16g
(3)解:设稀盐酸中氯化氢的质量为x,
NaOH+ | HCl═NaCl+H2O, |
40 | 36.5 |
16g×5% | x |
![]() =
= ![]() ,
,
x=0.73g,
稀盐酸中溶质的质量分数为: ![]() ×100%=7.3%,
×100%=7.3%,
答:稀盐酸中溶质的质量分数为7.3%
【解析】解:(1)a点溶液中大量存在的离子有钠离子和氯离子. 故填:钠离子和氯离子.(2)当恰好完全反应时,消耗NaOH溶液的质量为16g.
故填:16g.
a点时,溶液的pH等于7,说明稀盐酸和氢氧化钠恰好完全反应生成氯化钠和水,溶液中大量存在的离子是钠离子和氯离子;
根据图中信息可以判断当恰好完全反应时,消耗NaOH溶液的质量;
根据氢氧化钠溶液质量、溶质质量分数可以计算氯化氢的质量,进一步可以计算稀盐酸中溶质的质量分数.

练习册系列答案
相关题目
【题目】区别下列各组物质,所选择的试剂或方法错误的是( )
选项 | 需区别的物质 | 选择的试剂或方法 |
A | 氢气与二氧化碳 | 点燃 |
B | 空气与氧气 | 带火星的木条 |
C | 红磷与白磷 | 取少量放在空气中同时加热 |
D | 氮气与二氧化碳 | 燃着的木条 |
A. A B. B C. C D. D