题目内容
 (2013?崇安区二模)长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体,为鱼提供氧气.过氧化钙与水反应除生成氧气外,还生成什么物质?课外兴趣小组决定对这一问题中进行探究,请你参与.
(2013?崇安区二模)长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体,为鱼提供氧气.过氧化钙与水反应除生成氧气外,还生成什么物质?课外兴趣小组决定对这一问题中进行探究,请你参与.Ⅰ.定性探究
[提出问题]过氧化钙与水反应除生成氧气外,还生成什么物质?
[猜想]另一生成物为氢氧化钙.
[进行试验]取适量过氧化钙放入试管中加适量水,向试管中滴加酚酞试液,液体
呈
红
红
色,则猜想成立.写出该反应的化学方程式2CaO2+2H2O=2Ca(OH)2+O2↑
2CaO2+2H2O=2Ca(OH)2+O2↑
.[意外发现]较长时间后,同学们发现滴入酚酞后变色了的液体颜色又变回无色,你
认为褪色的可能原因是
Ca(OH)2被空气中的CO2反应掉了
Ca(OH)2被空气中的CO2反应掉了
.II.定量探究
[提出问题]测定久置过氧化钙样品中碳酸钙的质量分数.
[查阅资料]过氧化钙放置在空气中,会变质产生氢氧化钙和碳酸钙两种杂质.
[测定方案]
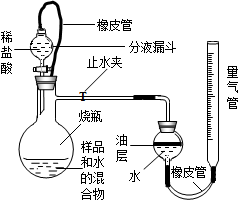
①如图所示,连接好装置,检查装置气密性良好;
②称量20g样品置于烧杯中,加入适量水混合,完全反应后全部倒入下图的烧瓶中,向分液漏斗中加入足量稀盐酸待用;
③将量气管液面调节到“0”刻度,并使量气管内液
面与油层相平,打开止水夹和分液漏斗活塞;
④反应结束后,再次调节量气管内液面与油层液面相
平,读出气体体积;
⑤查得CO2的密度,计算样品中碳酸钙的质量分数.
[问题讨论]
(1)图中油层的作用为
防止CO2溶于水
防止CO2溶于水
,中和反应明显放出热量,滴加稀盐酸后,发生装置里发生的中和反应的化学方程式为
Ca(OH)2+2HCl=CaCl2+2H2O
Ca(OH)2+2HCl=CaCl2+2H2O
,这个反应的发生可能使测定结果偏大
偏大
(填“偏大”、“偏小”或“不受影响”).(2)步骤②中将样品和水混合的目的是
除去CaO2,防止在烧瓶中产生氧气
除去CaO2,防止在烧瓶中产生氧气
.(3)反应结束后,测得量气管读数为1120ml,根据该条件下CO2的密度得知生成CO2
的质量为2.2g,求样品中碳酸钙的质量分数.(写出计算过程)
(4)充分反应后将烧瓶中的液体蒸干,得到27.75g固体,这袋样品在变质前全是过
氧化钙,其质量为
18
18
g.分析:【进行实验】根据实验探究的过程和学过的知识可知:酚酞试液遇到碱性溶液变成红色;过氧化钙与水反应生成氢氧化钙和氢气,写出反应的方程式;
【意外发现】较长时间后,同学们发现滴入酚酞后变色了的液体颜色又变回无色,是因为Ca(OH)2被空气中的二氧化碳反应掉了;
(1)根据二氧化碳易溶于水分析油层的作用;氢氧化钙和盐酸反应生成氯化钙和水,此过程是放热反应,造成气体体积膨胀,因此结果偏大;
(2)根据CaO2会和水反应产生氧气,会影响实验结果;
(3)根据二氧化碳的质量计算碳酸钙的质量和质量分数;
(4)根据得到27.75g固体为氯化钙,可以求钙元素的质量,反应前后元素的质量不变,然后求过氧化钙的质量.
【意外发现】较长时间后,同学们发现滴入酚酞后变色了的液体颜色又变回无色,是因为Ca(OH)2被空气中的二氧化碳反应掉了;
(1)根据二氧化碳易溶于水分析油层的作用;氢氧化钙和盐酸反应生成氯化钙和水,此过程是放热反应,造成气体体积膨胀,因此结果偏大;
(2)根据CaO2会和水反应产生氧气,会影响实验结果;
(3)根据二氧化碳的质量计算碳酸钙的质量和质量分数;
(4)根据得到27.75g固体为氯化钙,可以求钙元素的质量,反应前后元素的质量不变,然后求过氧化钙的质量.
解答:解:【进行实验】酚酞试液遇到碱性溶液变成红色;过氧化钙与水反应生成氢氧化钙和氧气,反应的方程式为:2CaO2+2H2O=2Ca(OH)2+O2↑;
【意外发现】较长时间后,同学们发现滴入酚酞后变色了的液体颜色又变回无色,说明溶液不在呈现碱性,是因为Ca(OH)2被空气中的二氧化碳反应掉了;
(1)因为二氧化碳易溶于水,因此油层的作用是防止CO2溶于水;氢氧化钙和盐酸反应生成氯化钙和水,反应的方程式为:Ca(OH)2+2HCl=CaCl2+2H2O;因为此过程是放热反应,造成气体体积膨胀,因此结果偏大;
(2)因为CaO2会和水反应产生氧气,会影响实验结果,因此将样品和水混合的目的是:除去CaO2,防止在烧瓶中产生氧气;
(3)根据二氧化碳的质量计算碳酸钙的质量和质量分数;
(4)得到27.75g固体为氯化钙,其中钙元素的质量为:27.75g×
×100%=10g,因为反应前后元素的质量不变,因此过氧化钙的质量为:10g÷
×100%=18g.
故答案为:【进行实验】红; 2CaO2+2H2O=2Ca(OH)2+O2↑;
【意外发现】Ca(OH)2被空气中的CO2反应掉了;
(1)防止CO2溶于水; Ca(OH)2+2HCl=CaCl2+2H2O; 偏大;
(2)除去CaO2,防止在烧瓶中产生氧气;
(3)解:设碳酸钙的质量为x (格式若不正确,全对情况下扣 1分,不全对不扣分)
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2g
=
x=5g
样品中碳酸钙的质量分数=
×100%=25%
答:样品中碳酸钙的质量分数为25%.
(4)18 g.
【意外发现】较长时间后,同学们发现滴入酚酞后变色了的液体颜色又变回无色,说明溶液不在呈现碱性,是因为Ca(OH)2被空气中的二氧化碳反应掉了;
(1)因为二氧化碳易溶于水,因此油层的作用是防止CO2溶于水;氢氧化钙和盐酸反应生成氯化钙和水,反应的方程式为:Ca(OH)2+2HCl=CaCl2+2H2O;因为此过程是放热反应,造成气体体积膨胀,因此结果偏大;
(2)因为CaO2会和水反应产生氧气,会影响实验结果,因此将样品和水混合的目的是:除去CaO2,防止在烧瓶中产生氧气;
(3)根据二氧化碳的质量计算碳酸钙的质量和质量分数;
(4)得到27.75g固体为氯化钙,其中钙元素的质量为:27.75g×
| 40 |
| 111 |
| 40 |
| 72 |
故答案为:【进行实验】红; 2CaO2+2H2O=2Ca(OH)2+O2↑;
【意外发现】Ca(OH)2被空气中的CO2反应掉了;
(1)防止CO2溶于水; Ca(OH)2+2HCl=CaCl2+2H2O; 偏大;
(2)除去CaO2,防止在烧瓶中产生氧气;
(3)解:设碳酸钙的质量为x (格式若不正确,全对情况下扣 1分,不全对不扣分)
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2g
| 100 |
| x |
| 44 |
| 2.2g |
样品中碳酸钙的质量分数=
| 5g |
| 20g |
答:样品中碳酸钙的质量分数为25%.
(4)18 g.
点评:本题属于信息题的考查,解题的关键是依据题目有关的信息结合相关的知识进行解析,这种题目的特点往往是起点高、落点低.

练习册系列答案
相关题目