题目内容
蜡烛(足量)在如图甲所示密封集气瓶内燃烧至熄火,测得瓶内氧气体积分数的变化如图乙所示。下列判断不正确的是

A.蜡烛刚进入集气瓶内比在空气中燃烧更剧烈
B.过程中瓶内物质总质量不断增加
C.瓶内氧气体积分数小于一定值时,蜡烛无法燃烧
D.蜡烛熄灭后瓶内已知的气体除了CO2还有氧气
 阅读快车系列答案
阅读快车系列答案化学小组的同学们在探究“分子运动”时,设计了如下几组实验:
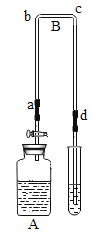
(实验装置)如图,实验1中的装置A取一个60 mL的试剂瓶,盖上一个单孔塞,单孔塞中插入一根带玻璃旋塞的导气管;装置B为一段医用输液管,内置一根浸泡过酚酞试剂并干燥的棉线。用橡胶管将A、B两装置链接。装置A 中加入约20 mL浓氨水,装置B的另一端连接导气管,导气管伸入小试管中。向小试管中加入一定量的蒸馏水。实验2、3、4的装置与实验1基本相同,只是根据实验需要变换了A、B装置和小试管的位置。
(实验步骤)①打开玻璃旋塞,观察现象。②将棉线润湿。
实验1 | 实验2 | 实验3 | 实验4 |
|
|
|
|
①干燥棉线没有明显变化。②湿润的棉线由a→b 逐渐匀速变红。 | 湿润的棉线由a→ b迅速变红,并且棉线变红的速率明显高于实验1 | 湿润的棉线由a→ b逐渐变红,并且棉线变红的速率明显低于实验1 装置。c→b 段棉线变红的速率比较缓慢,近b 端甚至不能变红。 | 湿润的棉线逐渐变红,并且a→b 段棉线变红的速率明显高于c→d 段棉线变红的速率 |
(1)以上实验得到的结论是:
①氨气不能使干燥的酚酞变色,氨气与水共同作用能够使酚酞试剂变红;
②_____;
③_____。
(2)若要应用实验1装置探究“温度对分子运动的影响”可以采取的操作是_____。
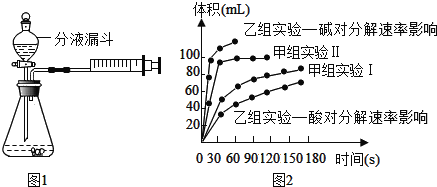
现甲、乙两化学小组安装两套如图1相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素。
(1)写出上述反应的化学方程式为_____。
(2)甲、乙小组设计如下实验设计方案。
实验编号 | 温度 | 等质量的催化剂 | 浓度 |
甲组实验I | 25℃ | 0.5g二氧化锰 | 10mL3.49%H2O2 |
甲组实验Ⅱ | 25℃ | 0.5g二氧化锰 | 10mL6.8%H2O2 |
实验编号 | 温度 | 等质量的催化剂 | 浓度 | 加入等浓度的试剂(各2mL) |
乙组实验I | 25℃ | 0.5g二氧化锰 | 10mL6.8%H2O2 | 氢氧化钠 |
乙组实验Ⅱ | 25℃ | 0.5g二氧化锰 | 10mL68%H2O2 | 硫酸 |
最终实验得到的结果如图2所示,回答下列问题:
①通过甲组实验得出的数据分析,得到的结论是_____;
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析:相同条件下,H2O2在_____(填“酸”或“碱”)性环境下放出气体速率较快。
(3)下列有关H2O2溶液,说法中不正确的是(____)
A H2O2溶液是混合物
B 5.1%的H2O2溶液中氢元素的质量分数为0.3%
C 二氧化锰并不是H2O2分解唯一的催化剂
D H2O2中氢分子和氧分子的个数比为1:1
(4)医学上常用过氧化氢溶液来清洗创口和局部抗菌。为了测定一瓶医用过氧化氢水溶液的溶质质量分数,取该过氧化氢溶液68.0g放入烧杯中然后称量得到108.8g,然后加入2.0g二氧化锰,完全反应后,再称量其质量为110.0g。请回答下列问题:
①生成的氧气为_____g;蒸干烧杯内液体,所得固体物质为_____g。
②试通过计算求该过氧化氢溶液中溶质的质量分数。_____(要有计算过程,结果精确到0.1%)


 2CO2+3H2O,根据该化学方程式无法获取的信息是
2CO2+3H2O,根据该化学方程式无法获取的信息是


 倾倒液体 B.
倾倒液体 B. 称量固体
称量固体 点燃酒精灯 D.
点燃酒精灯 D. 检查气密性
检查气密性