题目内容
【题目】甲,乙两位同学在学习甲烷性质时,发现甲烷与氢气和一氧化碳性质上有很多相似之处,如密度比空气小,难溶于水,具有可燃性等。H2和CO具有还原性,那么甲烷有没有还原性呢?为了验证甲烷是否具有还原性,乙同学设计如图所示装置并进行实验:
[实验装置]
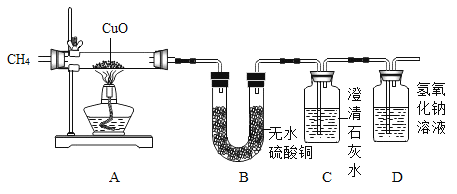
[实验步骤](假设药品都是足量的)
①分别称量装置A,B,C的质量;
②再次分别称量装置A,B,C的质量;
③向玻璃管中装入CuO,通入一段时间的CH4;
④停止加热,继续通入CH4至冷却到室温;
⑤缓缓通入足量的CH4,加热装置A,使其充分反应。
其合理的操作顺序是_____(填序号)。甲同学认为还缺少一个步骤,缺少的步骤是_____。
[进行实验]乙同学按照正确的步骤进行实验,并记录了实验现象和数据:
装置A中的黑色粉末变红;装置B中白色粉末变蓝;装置C中石灰水变浑浊;称量数据如表所示。
A中玻璃管(含药品)质量 | 装置B的质量 | 装置C的质量 | |
反应前 | 150 g | 156.6 g | 256.8 g |
反应后 | 147.2 g | 158.4 g | 257.9 g |
[现象分析与数据处理]
根据装置A,B,C中的现象可推知,CH4与CuO充分反应后的产物依次是_____。
[实验结论]
(1)CH4 _____(填“有”或“没有”)还原性;
(2)根据实验数据,甲同学提出甲烷与氧化铜反应的产物中还含有_____;
(3)装置A中发生的反应化学方程式为_____。
【答案】①③⑤④② 检查装置的气密性 Cu、H2O、CO2 有 CO ![]()
【解析】
[实验步骤]
按照如图所示的装置连接仪器后,后需要检查装置的气密性,防止装置漏气从而干扰实验。根据实验需要通过质量的改变得出结论,因此需要先分别称量装置A,B,C的质量。向玻璃管中装入CuO,通一段时间的CH4,以排净装置内的空气,防止加热时发生爆炸。然后缓缓通入足量的CH4,加热装置A,使其充分反应。等反应完再停止加热,继续通入CH4至冷却到室温,防止铜重新被氧化。最后再次分别称量装置A,B,C的质量,通过数据的变化进行计算。所以顺序为①③⑤④②。故答案为:①③⑤④②、检查装置的气密性;
[现象分析与数据处理]
装置A中的黑色粉末变红,证明生成了铜。装置B中白色粉末变蓝,证明生成了水。装置C中石灰水变浑浊,证明生成了二氧化碳。则可以推测出充分反应后的产物依次是Cu、H2O、CO2。故答案为:Cu、H2O、CO2;
[实验结论]
(1)通入甲烷后,氧化铜被还原为铜单质,则可以证明出甲烷、一氧化碳、氢气都具有还原性。故答案为:有;
(2)根据质量守恒定律可知,生成二氧化碳中碳元素的质量为:(257.9g-256.8g)×![]() =0.3g。生成的水中氢元素的质量为:(158.4g-156.6g)×
=0.3g。生成的水中氢元素的质量为:(158.4g-156.6g)×![]() =0.2g。则碳、氢元素的质量比为:0.3g:0.2g=3:2。而甲烷中,C:H=4:1,因此可知,还生成了一氧化碳。故答案为:CO;
=0.2g。则碳、氢元素的质量比为:0.3g:0.2g=3:2。而甲烷中,C:H=4:1,因此可知,还生成了一氧化碳。故答案为:CO;
(3)通过实验及计算可知,甲烷和氧化铜加热生成了铜、水、二氧化碳和一氧化碳,所以反应的方程式为:![]() 。
。

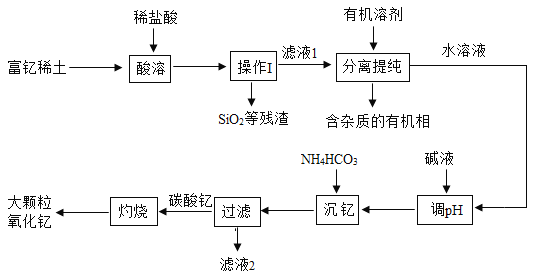
【题目】某化工厂为综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了制备(NH4)2SO4的工艺流程.
(工艺流程及原理)
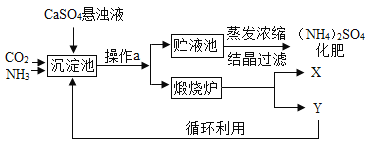
沉淀池中发生的主要化学反应为:CO2+2NH3+CaSO4+H2O=CaCO3↓+(NH4)2SO4
(讨论交流)
(1)操作a的名称是______,若在实验室进行此操作,用到的玻璃仪器除玻璃棒、烧杯外,还需要______。
(2)经操作a后得到的固体物质在煅烧炉中高温分解生成X和Y两种物质,该工艺中,Y被作为原料之一循环利用.Y的化学式为______。
(3)沉淀池中也可能生成少量NH4HCO3,该反应的化学方程式为______。
(硫酸铵化肥等级测定)
(1)判断(NH4)2SO4化肥中有无NH4HCO3:取少量试样溶于水,滴加足量的______,无气泡产生,则可判断该化肥中不存在NH4HCO3。
(2)化肥中氮元素含量的测定(已确定该化肥中不存在NH4HCO3杂质):
(查阅资料)
①已知:![]() ,氨气极易溶于水,其水溶液为氨水.氨水呈碱性,不稳定,易挥发.
,氨气极易溶于水,其水溶液为氨水.氨水呈碱性,不稳定,易挥发.
②工业判断硫酸铵化肥等级指标如下:
指标 项目 | 优等品 | 合格品 |
氮(N)含量 | ≥21.0% | ≥20.5% |
(实验设计)
按图所示装置进行实验.
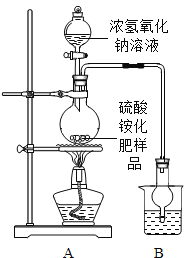
(1)实验过程中,往烧瓶中加入足量浓氢氧化钠溶液,并加热使硫酸铵充分反应完全转化为NH3.
(2)烧杯中的试剂是为了吸收产生的氨气,下列最适宜的试剂是______(填序号);
①水;②浓HCl;③稀H2SO4;④NaOH溶液
烧杯中干燥管的作用是______。
(交流讨论)
实验小组的同学认为,用上述实验装置测得的结果可能会出现下列情况.
(1)甲同学认为:应在实验装置A、B之间增加一个装有______(填“浓硫酸“或“碱石灰”)的干燥装置,否则实验测得的硫酸铵化肥含氮量可能偏高.
(2)乙同学认为:在实验装置A、B之间增加正确的干燥装置后进行实验,测得的硫酸铵化肥含氮量可能偏低,理由是______。
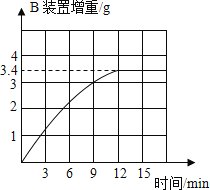
(实验测定)
经讨论后,他们改进了实验装置,排除了可能产生误差的因素,重新进行实验。取硫酸铵化肥样品13.5 g进行实验,测得B装置增重与反应时间的关系如图所示.请通过计算判断该化肥的等级.计算过程:_____;该化肥的等级为______品。