题目内容
【题目】小明家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬。好奇的小明想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加。
[作出猜想]猜想一:Cr>Fe>Cu; 想二: Fe>Cr>Cu; 猜想三:你的猜想是_____。
[查阅资料] (1) 铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4) 溶液。
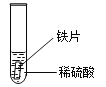
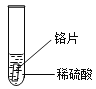
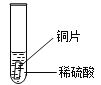
[设计实验]小明同学取大小相同的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸。
实验 | 试管1 | 试管2 | 试管3 |
实验操作 |
|
|
|
实验现象 | 铁片表面产生气泡较慢,溶液变为_____。 | 铬片表面产生气泡较快,溶液变为蓝色 | 铜片表面不产生气泡 |
[结论与解释]
(1)小明得到的结论是猜想_____正确。
(2)实验前用砂纸打磨金属片的目的是_____。
[拓展应用]将铬片投入CuSO4溶液中,反应_____(填“能”或“不能”)进行。若能进行,请你写出反应的化学方程式_____。
【答案】Fe>Cu>Cr 浅绿色 一 除去金属表面的氧化物 能 ![]()
【解析】
[作出猜想] 探究铬与铁、铜的活动性强弱,有3种可能性:①Cr>Fe>Cu、②Fe>Cr>Cu、③Fe>Cu>Cr;
故填:Fe>Cu>Cr。
[设计实验]试管1中,铁与稀硫酸反应时铁的表面产生气泡较慢,溶液由无色变为浅绿色;试管2中,铬片放到稀硫酸中,铬片表面产生气泡较快,溶液变为蓝色,说明铬比铁活泼,铬、铁在氢前面;试管3中,铜片放到稀硫酸中,铜片不与稀硫酸反应,说明铜在氢的后面;
故填:浅绿色。
[结论与解释]
(1)由上述实验,可验证出铬比铁活泼,铁比铜活泼,即:Cr>Fe>Cu;小明得到的结论是猜想一正确;
故填:一。
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化物,使金属与酸反应;
故填:除去金属表面的氧化物。
[拓展应用]将铬片投入CuSO4溶液中,铬比铜活泼,能发生反应,反应的化学方程式是![]() ;
;
故填:能;![]() 。
。

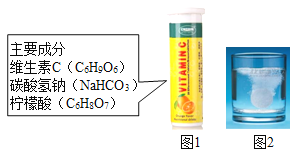
【题目】维C泡腾片是-种含有大量维生素C的片状物品,其成分见图1.将它加入水中,观察到产生许多气泡(图2)。某实验小组对该气体的成分进行了如下探究。
[猜想与假设]
备选的常见气体有五种,分别是: CO2、 O2、CO、H2、N2。
(1)小明认为:不可能含有N2,依据是_____。
(2)小芳认为:不可能含有CO和H2,理由是:从安全角度考虑,两种气体都易燃、易爆,而且CO_____。
经过讨论,小组同学认为:该气体可能含有CO2、O2 中的一种或两种。
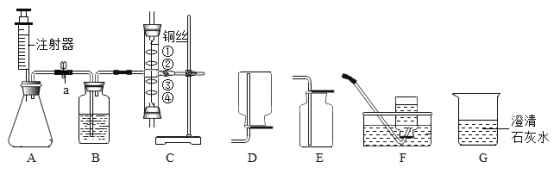
[进行实验]
实验编号 | 实验操作 | 实验现象 |
① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
② | 将带火星的木条伸入该气体中 | 木条没有复燃 |
[结论与评价]
(3)分析实验①可知,该气体中肯定含有_____。
(4)分析实验②不能确定该气体中是否含有氧气,理由是_____。
[补充探究]
(5)为了确定是否存在氧气,请补充设计实验。
实验步骤 | 现象与结论 |
_____ | _____ |