题目内容
【题目】通过学习,你已掌握了实验室制取气体的有关知识。请结合如图回答问题:
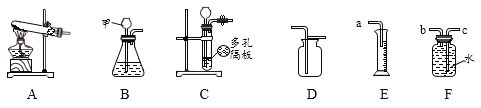
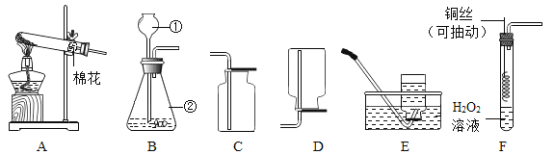
(1)仪器甲的名称是_____________。
(2)实验室加热高锰酸钾制取氧气应选用的发生装置为________(填字母),反应的化学方程式为:_____________________。某同学用D装置收集氧气,验满方法是______________________。如果要做铁丝在氧气中燃烧的实验,收集氧气时要在瓶底留一些水,其原因是______________________。
(3)实验室可用B或C装置制取二氧化碳,选用C相对于B装置的主要优点是_________________。可用澄清石灰水检验二氧化碳,反应的化学方程式为:__________,将制得的二氧化碳气体通入紫色石蕊溶液,观察到的现象是_________________。
(4)某同学用E、F装置收集一定量的氢气,装置接口连接的顺序为_________(填接口字母),量筒的作用是__________。
【答案】长颈漏斗 A 2KMnO4![]() K2MnO4+ MnO2+O2↑ 用带火星的木条放在集气瓶口,观察木条是否复燃,若复燃说明已收集满,反之则没有收集满 防止生成的高温熔融物溅落瓶底,使集气瓶炸裂 能控制反应的发生或停止 CO2+Ca(OH)2= CaCO3↓+H2O 溶液变红 bca 测量收集到的氢气体积
K2MnO4+ MnO2+O2↑ 用带火星的木条放在集气瓶口,观察木条是否复燃,若复燃说明已收集满,反之则没有收集满 防止生成的高温熔融物溅落瓶底,使集气瓶炸裂 能控制反应的发生或停止 CO2+Ca(OH)2= CaCO3↓+H2O 溶液变红 bca 测量收集到的氢气体积
【解析】
(1)仪器甲是长颈漏斗,故填长颈漏斗;
(2)高锰酸钾是固体,反应需要加热,选固体加热型装置,故填A,高锰酸钾受热反应生成锰酸钾、二氧化锰和氧气,方程式故填2KMnO4![]() K2MnO4+ MnO2+O2↑,采用排空气法收集氧气,验满时用带火星的木条放在集气瓶口,故填用带火星的木条放在集气瓶口,观察木条是否复燃,若复燃说明已收集满,反之则没有收集满;实验室在做铁丝在氧气中燃烧实验时,通常在集气瓶里放一些水或沙子,防止生成的高温熔融物溅落瓶底,使集气瓶炸裂,故填防止生成的高温熔融物溅落瓶底,使集气瓶炸裂;
K2MnO4+ MnO2+O2↑,采用排空气法收集氧气,验满时用带火星的木条放在集气瓶口,故填用带火星的木条放在集气瓶口,观察木条是否复燃,若复燃说明已收集满,反之则没有收集满;实验室在做铁丝在氧气中燃烧实验时,通常在集气瓶里放一些水或沙子,防止生成的高温熔融物溅落瓶底,使集气瓶炸裂,故填防止生成的高温熔融物溅落瓶底,使集气瓶炸裂;
(3)利用装置C中的多孔隔板,能随时控制反应的发生或停止,故填能控制反应的发生或停止;二氧化碳能使澄清石灰水变浑浊,是生成了难溶于水的碳酸钙和水,方程式故填CO2+Ca(OH)2= CaCO3↓+H2O;二氧化碳能和水反应生成碳酸,碳酸能使紫色石蕊溶液变红,故填溶液变红;
(4)用E、F装置收集定量氢气时,排水法收集氢气时应该是b口进氢气,c口排水,E装置是测量排出水的体积也即测量收集到的氢气体积,连接口顺序故填bca;量筒的作用故填测量收集到的氢气体积。

 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案【题目】小明同学欲通过实验证明“二氧化锰是氯酸钾受热分解的催化剂”这一命题。他设计并完成了下表所示的探究实验:
实验操作 | 实验现象 | 实验结论或总结 | ||
各步骤结论 | 总结 | |||
实验一 | 将氯酸钾加热至融化,伸入带火星的木条。 | 木条复燃 | 氯酸钾受热能分解产生氧气,但是速度较慢。 | 二氧化锰是氯酸钾受热分解的催化剂。 |
实验二 | 加热二氧化锰,伸入带火星的木条。 | 木条不复燃 | 二氧化锰受热不产生氧气。 | |
实验三 | 加热氯酸钾与二氧化锰的混合物 | 木条迅速复燃 | 二氧化锰能加快氯酸钾的分解。 | |
(1)在小明不同的探究实验中,实验一和实验二起的作用是__________;
(2)你认为由上述实验能完全得出表内“总结”吗?________(填“能或不能”),其理由是:一、___________;二、____________。
(3)某学生将一定质量的氯酸钾分成a、b两等分,他在a中加入少量二氧化锰混合均匀后将其装入试管中,另一份b直接装入试管中,然后按照要求架设好装置进行氧气的制取.其制取氧气的情况如图所示:
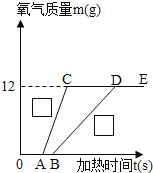
曲线缓则反应慢、曲线陡则反应快,试将a、b标在图中的“□”中_________、______;
点A、点B表示_________,点C、点D表示_________(填“反应开始”或“反应结束”).
OA、OB表示反应前所需的加热时间,依据OB>OA可看出催化剂二氧化锰的存在不仅可以加快化学反应速率,而且还可以______.
图中a、b两种情况的最终氧气产量均为12g,说明催化剂只能改变化学反应速率,不能改变____.