题目内容
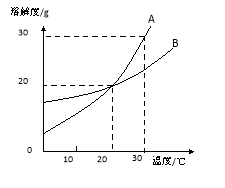
【题目】胆矾晶体部分失水后得到某硫酸铜晶体(CuSO4·xH2O),华雪同学为研究CuSO4·xH2O加热后所得物质的组成,做了以下实验:取10.7gCuSO4·xH2O晶体加热使其分解,绘制出固体的质量随温度的变化关系图。如图所示,到t1℃时该固体完全失去结晶水,化学方程式为:CuSO4·xH2O ![]() CuSO4+ xH2O↑
CuSO4+ xH2O↑

(1)计算该硫酸铜晶体(CuSO4·xH2O)中x的值。(CuSO4·x H2O的相对分子质量为:160+18x)
(2)CuSO4中铜元素的质量分数是多少?
(3)升温到t2℃,残留固体是黑色物质,则m为多少g。(写出求m的过程)
【答案】(1) CuSO4·xH2O ![]() CuSO4+ xH2O↑
CuSO4+ xH2O↑
160 18x
8.0g (10.7-8.0)g
160∶8.0 g =18x∶(10.7-8.0)g 解得:x=3
(2)CuSO4中铜元素的质量分数=![]() ×100%=40%
×100%=40%
(3)由题意知,升温到t2℃时,残留的黑色物质为CuO,依据质量守恒定律,CuSO4与CuO之间存在如下关系:CuSO4∽CuO
160 80
8.0g m g
160∶8.0 g=80∶m g 解得:m=4.0
【解析】试题分析:(1) CuSO4·xH2O![]() CuSO4+ xH2O↑
CuSO4+ xH2O↑
160 18x
8.0g (10.7-8.0)g
160∶8.0 g =18x∶(10.7-8.0)g 解得:x=3
(2)CuSO4中铜元素的质量分数=![]() ×100%=40%
×100%=40%
(3)由题意知,升温到t2℃时,残留的黑色物质为CuO,依据质量守恒定律,CuSO4与CuO之间存在如下关系:CuSO4∽CuO
160 80
8.0g m g
160∶8.0 g=80∶m g 解得:m=4.0

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】测定人体内或排出的液体pH,可以帮助人们了解身体的健康状况。人体内的一些液体的近似pH如下:
液体 | 胃液 | 胰液 | 胆汁 | 血浆 |
pH | 0.9-1.5 | 7.5-8.0 | 7.1-7.3 | 7.35-7.45 |
下列液体中,碱性最强的是( )
A.胃液 B. 胰液 C. 胆汁 D. 血浆