题目内容
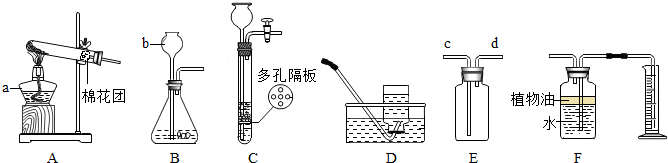
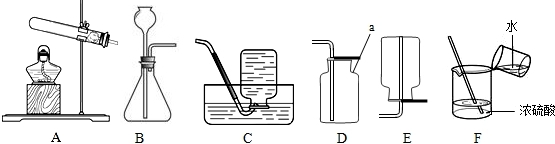
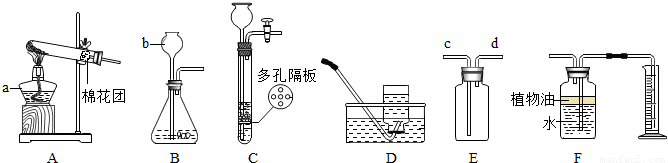
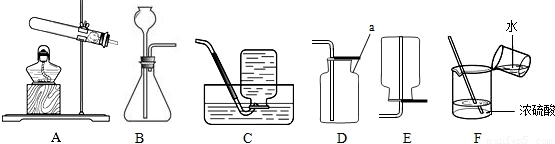
15、学习了气体的制取相关知识后,老师让小芳和同学成立一个化学兴趣小组,制备一定量的氢气.装置从下图中选择;实验室中的药品有:两种已经生锈的铜丝和铁丝,浓硫酸.
(1)首先,小芳和同学们准备用蒸馏水稀释浓硫酸制备稀硫酸,如图F为他们稀释浓硫酸的操作,该操作中的错误是
(2)请你帮助他们选择一种合适的金属来制取氢气,并写出用化学方法除去该金属表面的锈的化学反应方程式:
(3)仪器a名称是:
(4)小孩子常喜欢玩耍充满氢气的气球,但当氢气球从手中脱离的话,氢气球会十分迅速地升上高空,据此,你认为,在收集氢气的时候,应该选择的装置是

(1)首先,小芳和同学们准备用蒸馏水稀释浓硫酸制备稀硫酸,如图F为他们稀释浓硫酸的操作,该操作中的错误是
把水加入到浓硫酸中
.(2)请你帮助他们选择一种合适的金属来制取氢气,并写出用化学方法除去该金属表面的锈的化学反应方程式:
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
,然后用该金属与稀硫酸反应制取氢气,反应的化学方程式为Fe+H2SO4=FeSO4+H2↑
.(3)仪器a名称是:
集气瓶
,他们应选择的气体发生装置是B
(填字母序号,后同).(4)小孩子常喜欢玩耍充满氢气的气球,但当氢气球从手中脱离的话,氢气球会十分迅速地升上高空,据此,你认为,在收集氢气的时候,应该选择的装置是
E
.分析:(1)根据稀释浓硫酸的方法进行解答;
(2)根据铁和铜的金属活动性进行解答;
(3)根据发生装置选择依据进行解答;
(4)根据氢气的密度确定收集方法.
(2)根据铁和铜的金属活动性进行解答;
(3)根据发生装置选择依据进行解答;
(4)根据氢气的密度确定收集方法.
解答:解:(1)稀释浓硫酸时一定要把浓硫酸沿器壁慢慢注入水中,并不断搅拌,切不可把水倒入浓硫酸中,会造成液体飞溅造成事故;
(2)在金属活动性顺序表中,铁排在氢的前面,铜排在氢的后面,故选择铁与酸反应制氢气Fe+H2SO4=FeSO4+H2↑
,根据铁锈主要成分氧化铁与稀硫酸反应的生成物可写出化学方程式:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
(3)铁为固体,稀硫酸为液体,反应条件是常温,故选B发生装置;
(4)氢气的密度比空气小,故可用向下排空气法收集.
故答案为:
(1)把水加入到浓硫酸中
(2)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O; Fe+H2SO4=FeSO4+H2↑
(3)集气瓶B
(4)E
(2)在金属活动性顺序表中,铁排在氢的前面,铜排在氢的后面,故选择铁与酸反应制氢气Fe+H2SO4=FeSO4+H2↑
,根据铁锈主要成分氧化铁与稀硫酸反应的生成物可写出化学方程式:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
(3)铁为固体,稀硫酸为液体,反应条件是常温,故选B发生装置;
(4)氢气的密度比空气小,故可用向下排空气法收集.
故答案为:
(1)把水加入到浓硫酸中
(2)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O; Fe+H2SO4=FeSO4+H2↑
(3)集气瓶B
(4)E
点评:本题考查了浓硫酸的稀释、金属活动性顺序及发生装置、气体装置的选择依据.明确氢前金属能与酸反应,氢后金属不能与酸反应.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目