题目内容
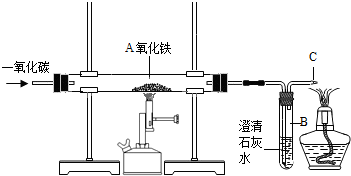
(2012?雅安)某探究小组拟在实验室用如图所示装置和药品制取气体:

请回答下列问题:
(1)A装置中收集气体的仪器名称是
(2)能够实现气体发生和收集的正确装置是
(3)某研究小组拟用装置A中的发生装置产生CO2.实验时需要溶质质量分数为9.8%的稀硫酸138g,则需要用

请回答下列问题:
(1)A装置中收集气体的仪器名称是
集气瓶
集气瓶
.(2)能够实现气体发生和收集的正确装置是
C
C
.该装置中制气体的反应方程式是2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
(3)某研究小组拟用装置A中的发生装置产生CO2.实验时需要溶质质量分数为9.8%的稀硫酸138g,则需要用
10
10
mL量筒一次性量取溶质质量分数为98%,密度为1.84g/mL的浓硫酸7.5
7.5
mL(准确到小数点后一位),才能配制出该稀硫酸.分析:(1)稀硫酸与氢氧化钠固体反应,生成的气体是二氧化碳,用集气瓶收集.
(2)A中生成的气体是二氧化碳,不可用向下排空气法收集;B中锌粒与稀盐酸反应,生成的气体是氢气,应该用向下排空气法收集;C中的双氧水和二氧化锰反应生成的气体是氧气,应该用向下排空气法收集;D中稀盐酸和石灰石反应,生成二氧化碳,应用向上排空气法收集.
(3)根据提供的数据,先计算出实验时需要溶质质量分数为9.8%的稀硫酸138g,中含有的硫酸的质量,再根据浓硫酸的密度计算出所需浓硫酸的体积,然后确定所用量筒.
(2)A中生成的气体是二氧化碳,不可用向下排空气法收集;B中锌粒与稀盐酸反应,生成的气体是氢气,应该用向下排空气法收集;C中的双氧水和二氧化锰反应生成的气体是氧气,应该用向下排空气法收集;D中稀盐酸和石灰石反应,生成二氧化碳,应用向上排空气法收集.
(3)根据提供的数据,先计算出实验时需要溶质质量分数为9.8%的稀硫酸138g,中含有的硫酸的质量,再根据浓硫酸的密度计算出所需浓硫酸的体积,然后确定所用量筒.
解答:解:(1)稀硫酸与氢氧化钠固体反应,生成的气体是二氧化碳,用集气瓶收集.
故答案为:集气瓶.
(2)A中生成的气体是二氧化碳,不可用向下排空气法收集,所以图中收集方法不正确;B中锌粒与稀盐酸反应,生成的气体是氢气,应该用向下排空气法收集,所以收集的方法不正确;C中的双氧水和二氧化锰反应生成的气体是氧气,应该用向上排空气法收集,收集方法正确,反应方程式是:2H2O2
2H2O+O2↑;D中稀盐酸和石灰石反应,生成二氧化碳,应用向上排空气法收集,收集方法不正确.
故答案为:C;2H2O2
2H2O+O2↑.
(3)实验时需要溶质质量分数为9.8%的稀硫酸138g,其中硫酸的量是:138×9.8%=13.5g.
所以需要溶质质量分数为98%的浓硫酸:13.5÷98%=13.8g
根据公式:m=ρ?v 可知需要取溶质质量分数为98%,密度为1.84g/mL的浓硫酸:v=
=
=7.5mL.所以要选用10mL的量筒.
故答案为:10;7.5.
故答案为:集气瓶.
(2)A中生成的气体是二氧化碳,不可用向下排空气法收集,所以图中收集方法不正确;B中锌粒与稀盐酸反应,生成的气体是氢气,应该用向下排空气法收集,所以收集的方法不正确;C中的双氧水和二氧化锰反应生成的气体是氧气,应该用向上排空气法收集,收集方法正确,反应方程式是:2H2O2
| ||
故答案为:C;2H2O2
| ||
(3)实验时需要溶质质量分数为9.8%的稀硫酸138g,其中硫酸的量是:138×9.8%=13.5g.
所以需要溶质质量分数为98%的浓硫酸:13.5÷98%=13.8g
根据公式:m=ρ?v 可知需要取溶质质量分数为98%,密度为1.84g/mL的浓硫酸:v=
| m |
| ρ |
| 13.8 |
| 1.84 |
故答案为:10;7.5.
点评:此题体现了学科直接的相互渗透,所以同学们要注意学科直接的均衡发展.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目