��Ŀ����
����Ŀ����Ȼ���ˮ���и������ʣ������ò�ͬ�ķ������о�����
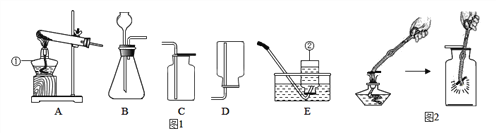
��1����ͼ��ʾ���ÿ���������ƿ�������ܵĵ������������ޡ�ɴ��������̿��С��ʯ��ʯӢɳ�Ȳ������Ƶ�һ������ˮ����
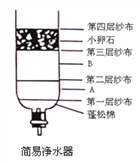
�ٸ��������������ϵ����ԣ�A����õIJ��������__________�����������˸����ʵ�___________��
������Ϊ��������ˮ��������ԡ������ԡ���________��Ӳ��Ӳˮ�����ˮ��
��2����ͼΪ����װ�ã�����ʵ��ش��������⣺
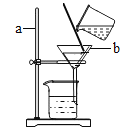
��ʵ������в�������������____________________ ��
�ڹ��˺�����Һ��Ȼ���ǣ����ܵ�ԭ����(���һ�㼴��)_____________________��
���𰸡� ����̿ ������ ������ ���� ��ֽ����
��������(1)������ˮ�IJ���������Ҫ�У����������ˡ������������������ˡ�������Ҫ��ȥ����ˮ�еIJ���������������ˮ���е�С��ʯ��ʯӢɳ������������ã�����Ӧ�ɴֵ�ϸ������С��ʯ���ˣ�����ʯӢɳ������A��װ���ǻ���̿����Ҫ���������ã�����������ˮ�е�ɫ�غ���ζ���ڶ����ɴ����Ҫ�ǰ�ʯӢɳ�ͻ���̿�������赲ʯӢɳ�������̿�У������������̿��������������2��������������������������Һ���ǵij���ԭ���У�1����ֽ����©���ڵ�Һ�������ֽ��Ե���н���Һ���ձ����ɾ��ȵȡ��⣺(1)�������������������ϵ����ԣ�A����õIJ�������ǻ���̿�����������˸����ʵ����������ڹ��ˡ�������Ҫ��ȥ����ˮ�еIJ��������ʣ�ˮ�л���������������ʣ������Խ�Ӳ��Ӳˮ�����ˮ����2�������ڹ���ʱ���ֱ������������㵹Һ�壬�ᵼ��Һ�彦����������ձ��ڽ����������㵹�Ļ���Һ��ͻ�˳�Ų��������£��Ӷ���������������ʲ������ڴ��������������������ֽ���𣬴����˵�Һ��ͻ���������£���ô��������ʧȥ�˹��˵����ã���õ�����Һ�ͻ������

 ��У����ϵ�д�
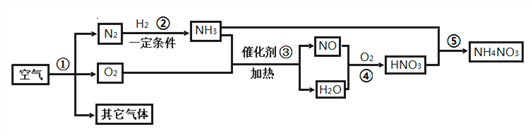
��У����ϵ�д�����Ŀ��ѧϰ��MnO2�Թ�������ֽ��д����õ�֪ʶ��ijͬѧ�룺Fe2O3�ܷ�������MnO2�Ĵ��������أ����ǽ���������̽����
�����롿����Fe2O3���Ǵ�����Ҳ�����뷴Ӧ����Ӧǰ�������ͻ�ѧ���ʲ��䣻
����Fe2O3���뷴Ӧ����O2����Ӧǰ�������ͻ�ѧ���ʷ����˱仯��
����Fe2O3�Ƿ�Ӧ�Ĵ�������Ӧǰ��_________________ ��
���������ϡ�Fe2O3���ڼ���������ܹ���ϡ���ᷴӦ�����Ȼ������Ȼ�����Һ���ػ�ɫ��
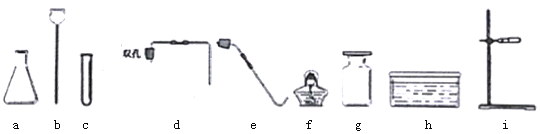
��ʵ�顿����ƽ����0.3gFe2O3��ȡ5mL5%�Ĺ���������Һ���Թ��У���������ʵ�飺
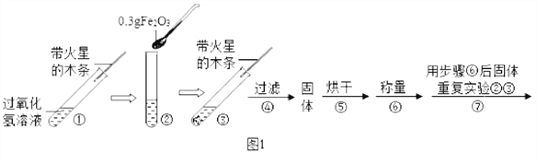
(1)������
��������� | ������ | ��������� | ���� |
________________�� �����ǵ�ľ����ȼ�� | _________________ | ��Һ��������ð���� _______________�� | ����������������������� |
(2)����ٵ�Ŀ����_____________________��
(3)��������õ���ʵ�������У�����̨(����Ȧ)��©�����ձ���_______ ��
(4)���������ܱ�Fe2O3���ֽ�ų������Ļ�ѧ����ʽΪ____________________��
����չ�� (1)Ҫ̽�����������������Fe2O3������ѧ���ʣ���Ӧ������ʵ����________��
(2)��ѧ��Ϊ�˼���̽��Fe2O3 ��������H2O2�ֽ����ʵ�Ӱ�죬ÿ�ξ���30mL10%��H2O2��Һ��ʹ�ò�ͬ������Fe2O3���������ⶨÿ���ռ���500mLO2���õ�ʱ�䡣���ͼ��ͼ(����ʵ��������ͬ)��
��ͼ��֪��Fe2O3 ��������H2O2�ֽ�����Ӱ��Ĺ����ǣ���___________________________ ��
��Fe2O3 ���������� һ����Χ��������������Ӧ���ʲ��ټ����ӿ졣