题目内容
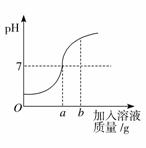
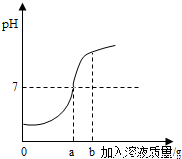
用质量分数为5%的稀盐酸和10%的氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如下图所示:
(1)该实验是将 (选填“稀盐酸”或“氢氧化钠溶液”)滴加到另一种溶液中。
(2)当加入溶液的质量a为20 g时,求所得溶液中溶质的质量。
【答案】
(1)氢氧化钠溶液 (1分)
(2)2.925 g (2分,结果2.9或2.93也可以)
【解析】此题通过对中和反应及其应用的知识考查了根据化学方程式进行计算。(1)开始时溶液的pH小于7,说明是把氢氧化钠溶液滴加到稀盐酸中;(2)当加入溶液的质量为a为20g时,溶液的pH等于7,说明盐酸和氢氧化钠刚好完全中和,此时所得溶液中的溶质为氯化钠。根据化学方程式进行计算即可。
解:设所得溶质质量为x
则 NaOH + HCl = NaCl + H2O
40 58.5
20×10% x
40/58.5 = 20×10%/x
X=2.925 g

练习册系列答案
相关题目
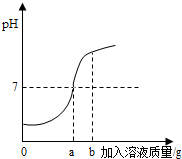 (2012?枣庄)用质量分数为5%的稀盐酸和10%的氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示:
(2012?枣庄)用质量分数为5%的稀盐酸和10%的氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示: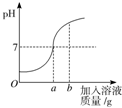 用质量分数为5%的稀盐酸和10%的氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如下图所示:
用质量分数为5%的稀盐酸和10%的氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如下图所示: