题目内容
【题目】【2016年江苏省苏州市】为测定某市售碳酸钙药品中碳酸钙的质量分数(杂质为SiO2,与稀盐酸不反应),某同学的方法是:将样品与稀盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中碳酸钙的质量,从而计算出样品中碳酸钙的质量分数。为测定生成CO2的质量,他设计了如下实验方案(已知:无水氯化钙是常见的干燥剂):
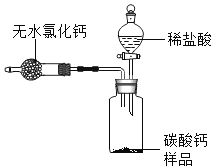
(1)按图组装好装置,检查装置气密性后,在分液漏斗中加入过量稀盐酸,并在干燥管中加入适量无水氯化钙样品,称得装置和药品的总质量为564.57g;
(2)在广口瓶中加入碳酸钙样品,称得装置和药品的总质量为574.57g;
(3)旋紧橡皮塞,打开分液漏斗旋塞,向广口瓶中滴加稀盐酸,使样品与稀盐酸完全反应;
(4)反应结束后,称得装置及装置内所有物质的总质量为570.57g。
请根据上述实验回答下列问题:
(1)该方案测得样品中碳酸钙的质量分数是多少(写出解题过程,计算结果精确到0.1%)?
(2)该实验中用稀盐酸与碳酸钙样品反应,而不用浓盐酸与碳酸钙样品反应,其原因是
。若实验中不用无水氯化钙干燥,则测得样品中碳酸钙的质量分数与上述实验计算结果相比 (选填“偏小”或“不变”或“偏大”)。
【答案】(1)90.9%(2)浓盐酸具有挥发性,会带来测量误差 偏大
【解析】
(1)样品的质量为:574.57g﹣564.57g=10g
生成二氧化碳的质量为:574.57g﹣570.57g=4g
设参加反应的碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4g
![]() =
=![]()
x=9.09g
所以碳酸钙样品中碳酸钙的质量分数为:![]() ×100%=90.9%;
×100%=90.9%;
(2)浓盐酸具有挥发性,所以在实验中用稀盐酸与碳酸钙样品反应,而不用浓盐酸与碳酸钙样品反应;实验中不用无水氯化钙干燥,会使排出的二氧化碳气体中含有水蒸气,导致结果偏大

