题目内容
12、根据下表中几种固体物质在水中的溶解度,判断下列说法正确的是( )
|
分析:A、依据溶解度的定义,确定溶质、溶剂、溶液之间的质量关系,查阅该温时此物质的溶解度,对照选项中的数据进行判断;
B、依据表格中的数据,查阅该温时此物质的溶解度,再由溶解度的定义,确定溶质、溶剂、溶液之间的质量关系,结合选项中的数据进行判断;
C、明确冷却热饱和溶液提纯物质的适用范围,对照两种物质的溶解度特点进行判断;
D、依据物质的溶解度变化特点确定降温时饱和溶液析出晶体还是变为不饱和溶液.
B、依据表格中的数据,查阅该温时此物质的溶解度,再由溶解度的定义,确定溶质、溶剂、溶液之间的质量关系,结合选项中的数据进行判断;
C、明确冷却热饱和溶液提纯物质的适用范围,对照两种物质的溶解度特点进行判断;
D、依据物质的溶解度变化特点确定降温时饱和溶液析出晶体还是变为不饱和溶液.
解答:解:A、查阅20℃时硝酸钾的溶解度为31.6g,由溶解度的定义可以确定,100g水恰好可溶解31.6g硝酸钾达到饱和,所得饱和溶液为131.6g,而选项中溶液为100g,故A错;
B、由表格中的数据较易查到20℃时氯化钠的溶解度为36g,由溶解度的定义可以确定,100g水恰好可溶解36g氯化钠达到饱和,选项中所给溶质为40g,会剩余4g不能溶解,只能得到136g溶液,故B错;
C、冷却热饱和溶液提纯物质的适用范围是:两种固体可溶物,其一溶解度受温度变化影响较大,另一种物质溶解度受温度变化影响较小,对照两种物质的溶解度特点恰好符合,故C对;
D、氯化钠的溶解度变化特点为:溶解度随着温度的升高而增大,当由80℃降至20℃时,氯化钠的溶解度由38.4g降至36g,所以会析出晶体,故D错.
故选C.
B、由表格中的数据较易查到20℃时氯化钠的溶解度为36g,由溶解度的定义可以确定,100g水恰好可溶解36g氯化钠达到饱和,选项中所给溶质为40g,会剩余4g不能溶解,只能得到136g溶液,故B错;
C、冷却热饱和溶液提纯物质的适用范围是:两种固体可溶物,其一溶解度受温度变化影响较大,另一种物质溶解度受温度变化影响较小,对照两种物质的溶解度特点恰好符合,故C对;
D、氯化钠的溶解度变化特点为:溶解度随着温度的升高而增大,当由80℃降至20℃时,氯化钠的溶解度由38.4g降至36g,所以会析出晶体,故D错.
故选C.
点评:该题考查的是溶解度问题,解答此类问题需做好几点:能由表格准确查阅一种物质的溶解度,理解溶解度的含义并明确饱和溶液中溶质、溶剂、溶液之间的质量关系,能由溶解度特点判断温度变化时溶液饱和情况的变化.

练习册系列答案
相关题目
张南、棒棒和多多同学学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体.但他在空气中点燃镁条时.却发现在生成的白色固体中还夹杂着少量的淡黄色固体及黑色颗粒.
提出问题:为什么固体会有其他颜色?
查阅资料:镁的几种化合物的颜色:
棒棒同学认为不必查阅氯化镁的颜色,理由是
提出猜想:分析资料,张南认为淡黄色固体可能是由镁与空气中的 反应生成的;
实验探究:为了确定MgO以外的其他成分,张南、棒棒和多多设计实验证实了自己的猜想.张南设计的方案如图l:

分析:2.4024 g Mg在足量纯氧中燃烧,理论上应生成MgO g.结合表中数据,可推断所得固体中,除MgO外 (填“存在”或“不存在”)其他物质.
棒棒设计的方案如图2:取少量所得样品于试管中,加少量水,出现白色沉淀,微热,发现有使湿润的红色石蕊试纸变蓝的气体生成,则此气体是 (填化学式),继续加足量水,仔细观察发现试管中除白色沉淀外,还有极少量的黑色不溶物.结合空气组成,棒棒推测样品中除MgO外还有
多多设计的方案如图3:先用足量的红磷做燃烧实验,冷却后,打开止水阀,结果发现烧杯中的水倒流人广口瓶中,倒流人的水的体积与广口瓶容积之比约为 ,此时瓶中剩余气体的主要成分为 (填化学式);关闭止水阀,取出连带橡皮塞的燃烧匙.迅速塞上备用橡皮塞.向燃烧匙中加入镁带并引燃,取下备用橡皮塞,将燃烧匙迅速插入瓶中,并将橡皮塞塞紧.发现镁带继续燃烧,产生黄色火焰,冷却后,打开止水阀,结果发现烧杯中的水依然倒流人广口瓶中,多多的结论是 .
实验结论:根据三位同学的实验,最终得出正确结论是:固体由 组成.
反思与评价:通过上述实验,你对燃烧的新认识是 .
提出问题:为什么固体会有其他颜色?
查阅资料:镁的几种化合物的颜色:
| 物 质 | MgO | MgCl2 | Mg2N3 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
提出猜想:分析资料,张南认为淡黄色固体可能是由镁与空气中的
实验探究:为了确定MgO以外的其他成分,张南、棒棒和多多设计实验证实了自己的猜想.张南设计的方案如图l:

| 反应前镁带的质量 | 反应的固体产物的质量 | |
| 第一次 | 2.4046g | 3.8854g |
| 第二次 | 2.4024g | 3.8839g |
| 第三次 | 2.4063g | 3.8857g |
棒棒设计的方案如图2:取少量所得样品于试管中,加少量水,出现白色沉淀,微热,发现有使湿润的红色石蕊试纸变蓝的气体生成,则此气体是
多多设计的方案如图3:先用足量的红磷做燃烧实验,冷却后,打开止水阀,结果发现烧杯中的水倒流人广口瓶中,倒流人的水的体积与广口瓶容积之比约为
实验结论:根据三位同学的实验,最终得出正确结论是:固体由
反思与评价:通过上述实验,你对燃烧的新认识是
(18分)以下是我们日常生活中常用的各种清洗剂,选择适当的用品可以得到更好的清洗效果。
| 名称 | 洗洁精 | 洁厕灵 | 炉具清洁剂 | 污渍爆炸盐 | 漂白粉 |
| 产品样式 |  |  |  |  |  |
| 有效成分 或功能 | 清洗油污 | 盐酸 | 氢氧化钠 | 过碳酸钠 | 消毒 |
(2)以下物质可以使用洁厕灵清洗的是 (填字母序号)。
a.铁锈 b.油渍 c.水垢(主要成分为碳酸钙和氢氧化镁)
(3)取上述一定量的炉具清洁剂,滴加几滴酚酞溶液,溶液变 色,若将洁厕灵与炉具清洁剂混合,可以发生下图所示的化学反应。图中a微粒的名称为 。

(4)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2。将爆炸盐溶于水后,再加入足量的洁厕灵,发生的化学反应方程式为 。
(5)化学小组发现一袋包装破损的漂白粉,同学们对漂白粉其漂白作用是否失效产生了疑问。(当有效成分完全消失时,则漂白粉就完全失效;部分消失时,则为部分失效)。
【查阅资料】
①漂白粉的主要成分是Ca(ClO)2、CaCl2和Ca(OH)2,其有效成分是Ca(ClO)2。
②Ca(ClO)2可溶于水,漂白原理是:它在空气中发生反应: Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO,

③ HClO不稳定,易分解生成HCl和一种常见的单质气体。
④ CaCl2的水溶液呈中性,HClO的水溶液呈酸性。
⑤ HClO能可使有色物质(如:品红溶液)褪色。
【实验探究】下表是探究某漂白粉是否完全失效的实验,请根据表中结论,进行填空。
| 实验步骤 | 实验现象 | 实验结论 |
| 把少量漂白粉样品加入水中,通入足量的CO2气体, 。 | | 漂白粉的漂白作用已完全失效 |
猜想一:CaCl2和CaCO3;猜想二: 。然后进行实验探究。
| 实验操作 | 实验现象 | 实验结论 |
| 把样品加入水中,充分溶解后过滤,_______________。 | ______________ | 猜想一成立 |
①HClO分解时除生成HCl外,生成的另一种常见气体是 。
②猜想中的成分CaCO3,除漂白粉的有效成分在空气中发生反应生成外,还有其它来源,请你用化学方程式表示 。
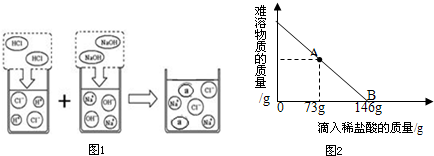
【定量研究】取上述漂白粉31.1g于一烧杯中,向其中加入131.7g水,使漂白粉中的可溶物完全溶解。然后再向其中逐滴加入溶质质量分数为10%的稀盐酸,烧杯中难溶固体物质的质量与所滴入稀盐酸的质量关系曲线如图所示。请根据题意回答下列问题:
①当滴入10%的稀盐酸至图中A点时,烧杯中溶液里含有的溶质是(写化学式)________。
②当滴入10%的稀盐酸146g时(即B点),试通过计算,求此时烧杯中所得不饱和溶液中溶质的质量分数。

回收废旧干电池、保护环境是我们每个公民的义务,下面是我校化学兴趣小组探究回收废旧于电池意义的过程(片断),请帮助他们完成相应报告。
[提出问题]废旧干电池的组成物质有什么(干电池的主要组成示意图见图)?

[活动探究]电池中含有的材料有哪些?请各举一例:金属 ;非金属 ;……
[活动探究2]电池的内容物中有没有我们熟悉的阴离子?
[猜想l]小组中一同学在剥开电池锌壳时,闻到一股淡淡的刺激性气味,因此他提出:电池的内容物中含有![]() 。
。
[设计方案l]取少量白色糊状物与![]() 固体混合置于试管中,加热,用 的红色石蕊试纸置于试管口,观察到 ,证明上述猜想正确。
固体混合置于试管中,加热,用 的红色石蕊试纸置于试管口,观察到 ,证明上述猜想正确。
[猜想2]可能含有![]() 、
、![]() 、
、![]() 、
、![]() 中的一种或几种。
中的一种或几种。
[设计方案2]为了验证猜想2,设计如下实验,请完成下表中相应内容。
[结论]上处实验证明,电池内白色糊状物主要是: (一种盐)和 等两种物质混合而成。
[交流与讨论]根据上述探究过程,你认为电池内容物有无回收价值?并请简要说明理由。
表1实验记录
| 操作步骤 | 实验现象 | 相应的结论 |
| 1、取样。溶于适量的水中,静置,过滤。取少量滤液于一支试管中,滴加紫色石蕊试液 | 石蕊试液不变蓝色 | ―― |
| 2、另取少量滤液于另一支试管中,滴加稍过量的 | 无明显现象 | 没有 |
| 3、再向第2步所得溶液中继续滴加少量的 溶液 |
| 没有 |
| 4、向第3步所得溶液中再滴加少量硝酸银溶液 | 有白色沉淀产生 | 有 存在 |
| 5、取白色糊状物,滴加少量碘液 | 有蓝色出现 | 则说明有 存在 |
(2008?南岗区二模)张南、棒棒和多多同学学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体.但他在空气中点燃镁条时.却发现在生成的白色固体中还夹杂着少量的淡黄色固体及黑色颗粒.
提出问题:为什么固体会有其他颜色?
查阅资料:镁的几种化合物的颜色:
棒棒同学认为不必查阅氯化镁的颜色,理由是______
提出猜想:分析资料,张南认为淡黄色固体可能是由镁与空气中的______反应生成的;
实验探究:为了确定MgO以外的其他成分,张南、棒棒和多多设计实验证实了自己的猜想.张南设计的方案如图l:
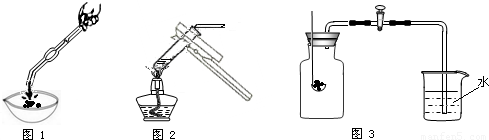
分析:2.4024 g Mg在足量纯氧中燃烧,理论上应生成MgO______g.结合表中数据,可推断所得固体中,除MgO外______(填“存在”或“不存在”)其他物质.
棒棒设计的方案如图2:取少量所得样品于试管中,加少量水,出现白色沉淀,微热,发现有使湿润的红色石蕊试纸变蓝的气体生成,则此气体是______(填化学式),继续加足量水,仔细观察发现试管中除白色沉淀外,还有极少量的黑色不溶物.结合空气组成,棒棒推测样品中除MgO外还有______
多多设计的方案如图3:先用足量的红磷做燃烧实验,冷却后,打开止水阀,结果发现烧杯中的水倒流人广口瓶中,倒流人的水的体积与广口瓶容积之比约为______,此时瓶中剩余气体的主要成分为______(填化学式);关闭止水阀,取出连带橡皮塞的燃烧匙.迅速塞上备用橡皮塞.向燃烧匙中加入镁带并引燃,取下备用橡皮塞,将燃烧匙迅速插入瓶中,并将橡皮塞塞紧.发现镁带继续燃烧,产生黄色火焰,冷却后,打开止水阀,结果发现烧杯中的水依然倒流人广口瓶中,多多的结论是______.
实验结论:根据三位同学的实验,最终得出正确结论是:固体由______组成.
反思与评价:通过上述实验,你对燃烧的新认识是______.
提出问题:为什么固体会有其他颜色?
查阅资料:镁的几种化合物的颜色:
| 物 质 | MgO | MgCl2 | Mg2N3 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
提出猜想:分析资料,张南认为淡黄色固体可能是由镁与空气中的______反应生成的;
实验探究:为了确定MgO以外的其他成分,张南、棒棒和多多设计实验证实了自己的猜想.张南设计的方案如图l:

| 反应前镁带的质量 | 反应的固体产物的质量 | |
| 第一次 | 2.4046g | 3.8854g |
| 第二次 | 2.4024g | 3.8839g |
| 第三次 | 2.4063g | 3.8857g |
棒棒设计的方案如图2:取少量所得样品于试管中,加少量水,出现白色沉淀,微热,发现有使湿润的红色石蕊试纸变蓝的气体生成,则此气体是______(填化学式),继续加足量水,仔细观察发现试管中除白色沉淀外,还有极少量的黑色不溶物.结合空气组成,棒棒推测样品中除MgO外还有______
多多设计的方案如图3:先用足量的红磷做燃烧实验,冷却后,打开止水阀,结果发现烧杯中的水倒流人广口瓶中,倒流人的水的体积与广口瓶容积之比约为______,此时瓶中剩余气体的主要成分为______(填化学式);关闭止水阀,取出连带橡皮塞的燃烧匙.迅速塞上备用橡皮塞.向燃烧匙中加入镁带并引燃,取下备用橡皮塞,将燃烧匙迅速插入瓶中,并将橡皮塞塞紧.发现镁带继续燃烧,产生黄色火焰,冷却后,打开止水阀,结果发现烧杯中的水依然倒流人广口瓶中,多多的结论是______.
实验结论:根据三位同学的实验,最终得出正确结论是:固体由______组成.
反思与评价:通过上述实验,你对燃烧的新认识是______.